
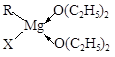 ②AB ③ABCD
②AB ③ABCD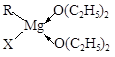 。
。

科目:高中化学 来源:不详 题型:单选题

| A.分子晶体中都存在共价键 |
| B.CaTiO3晶体中每个Ti4+和12个O2-相紧邻 |
| C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合 |
| D.熔融时化学键没有破坏的晶体一定是金属晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2和SiO2 | B.NaCl和HCl | C.CCl4和KCl | D.NH3和H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2O2分子中,两个O之间形成2对共用电子对 |
| B.N2的电子式是N┇┇N |
| C.CO2和CS2都是直线型分子 |
| D.白磷和甲烷都是正四面体型,键角都是109°28′ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在NaCl晶体中,与一个Na+最近的且距离相等的Cl-的个数 |
| B.在金刚石晶体中,围成最小环的原子数 |
| C.在二氧化硅晶体中,围成最小环的原子数 |
| D.在CsCl晶体中,与一个Cs+最近的且距离相等的Cs+的个数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH4↑+X(已配平)
CH4↑+X(已配平)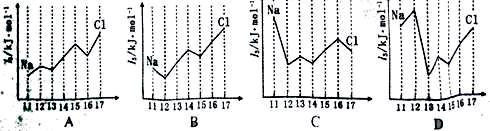
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属原子只有还原性而其阳离子只有氧化性 |
| B.金属阳离子只存于化合物中且有相应的阴离子相配合 |
| C.金属单质在常温下均为金属晶体 |
| D.某单质具有延展性则它一定是金属 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com