
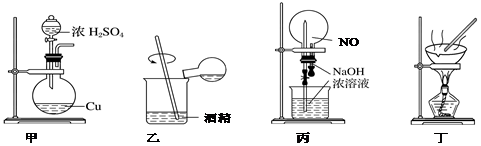
| A. | 用图甲做铜与浓硫酸反应制取SO2 | |
| B. | 用图乙配制浓硫酸与酒精的混合液 | |
| C. | 用图丙做NO与NaOH溶液的“喷泉”实验 | |
| D. | 用装置丁做蒸发CuCl2溶液获得CuCl2•2H2O |
分析 A.Cu与浓硫酸反应需要加热;
B.酒精的密度较小,需要将浓硫酸缓缓加入酒精中;
C.一氧化氮气体不与氢氧化钠溶液反应,无法完成喷泉实验;
D.HCl易挥发,加热过程中促进了铜离子的水解,图示操作无法获得CuCl2•2H2O.
解答 解:A.Cu与浓硫酸反应需要加热,图中缺少酒精灯,不能制取SO2气体,故A错误;
B.混合过程中放出大量热,且浓硫酸密度较大,需要将浓硫酸加入酒精中,可用图乙配制浓硫酸与酒精的混合液,故B正确;
C.NO不溶于水,也不与NaOH溶液反应,无法用图丙做NO与NaOH溶液的“喷泉”实验,故C错误;
D.蒸发CuCl2溶液时促进了铜离子的水解,由于HCl易挥发,最终得到的是氢氧化铜,无法获得CuCl2•2H2O,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握气体的制备及收集、浓硫酸的稀释方法及实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钙溶液加到醋酸溶液中:Ca(HCO3)2+2CH3COOH═Ca2++2CH3COO-+2CO2↑+2H2O | |
| B. | 漂白粉溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO3 | |
| C. | Fe-Cu-H2SO4溶液组成的原电池中负极反应式为:Fe-3e-=Fe3+ | |
| D. | 在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
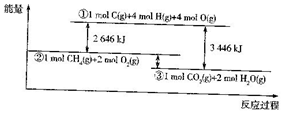 如图表示甲烷和氧气反应过程中的能量变化:请回答下列问题:
如图表示甲烷和氧气反应过程中的能量变化:请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 球棍模型: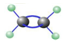 | B. | 分子中六个原子在同一平面上 | ||
| C. | 键角:109o28’ | D. | 碳碳双键中的一根键容易断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | ①中物质 | ②中的物质 | 预测②中的现象和结论 | 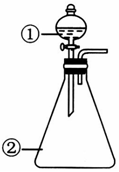 |
| A | 浓盐酸 | 二氧化锰 | 立即产生大量黄绿色气体,证明 HC1具有还原性和酸性 | |
| B | 草酸溶液 | 酸性高锰酸钾溶液 | 溶液逐渐褪色,证明草酸具有还原性 | |
| C | 硫酸铝饱和溶液 | 碳酸钠饱和溶液 | 立即产生大量气泡,证明两者相互促进水解 | |
| D | 蒸馏水 | 过氧化钠粉末 | 立即产生大量气泡,滴加酚酞溶液后变红,说明过氧化钠是碱性氧化物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.请回答下列问题:
碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚沾在手上应立即用酒精洗涤 | |
| B. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| C. | 点燃甲烷、乙烯等可燃性气体前必须先检验其纯度 | |
| D. | 在苯酚溶液中滴入少量稀溴水出现白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 离子组 | 加入试剂 | 离子方程式 | |
| A | Al3+、SO42- | 适量Ba(OH)2溶液 | Al3++3OH-═Al(OH)3↓ |
| B | Fe2+、I- | 足量新制氯水 | Cl2+2I-═2Cl-+I2 |
| C | Fe3+、NO3- | NaHSO3溶液 | 3SO32-+2NO3-+2H+═3SO42-+2NO↑+H2O |
| D | Ca2+、HCO3- | 氨水 | Ca2++2HCO3-+2NH3•H2O═CaCO3↓+CO32-+2NH4++2H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com