
【题目】可证明次氯酸是弱酸的事实是( )
A. 次氯酸可与碱反应 B. 次氯酸有漂白性
C. 次氯酸钙可与碳酸反应生成次氯酸 D. 次氯酸见光分解
科目:高中化学 来源: 题型:
【题目】浓盐酸和Ca(ClO)2能发生如下反应:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2十2H20用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是( )
A.CO2、HC1、H2O B.HC1、H2O、O2
C.HC1、H2O D.CO2、O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下三个实验方案以探究某反应是放热反应还是吸热反应:

方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10 mL 2 mol·L-1稀硫酸,再插入一支温度计,温度计的温度由20 ℃逐渐升至35 ℃,随后,温度逐渐下降至30 ℃,最终停留在20 ℃。
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10 mL 2 mol·L-1硫酸溶液,再向其中加入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来。
方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红墨水液面高低判断某反应是吸热反应还是放热反应。

根据上述实验回答相关问题:
(1)方案一中,温度先升高的原因是_________________,升至最大值后又逐渐下降的原因是 _____________________。
(2)方案二中,小木片脱落的原因是 ______________________。
(3)由方案三的现象得出结论:①③④组物质发生的反应都是________(填“吸热”或“放热”)反应 。
(4)方案三实验②的U形管中的现象为 ___________________,说明反应物的总能量________(填“大于”“小于”或“等于”)生成物的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在恒容密闭容器中发生如下反应:A(g)+2B(g)![]() 3C(g),若反应开始时充入2 molA和2molB,达平衡后A的体积分数为a%,其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
3C(g),若反应开始时充入2 molA和2molB,达平衡后A的体积分数为a%,其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
A. 2 mol C B. 1 molA、2molB和1molHe
C. 1 molA和 1 molC D. 3 molA、2 molB和3 mol C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应 | 平衡常数 | 温度℃ | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) | K3 | ||
(1)反应②是________________(填“吸热”或“放热”)反应。
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系,如左下图所示。则平衡状态由A变到B时,平衡常数K(A)_____________K(B)(填“>”、“<”或“=”)。据反应①与②可推导出K1、K2与K3之间的关系,则K3=_______(用K1、K2表示)。
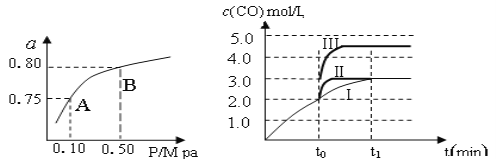
(3)在3 L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如右上图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。
当曲线Ⅰ变为曲线Ⅱ时,改变的条件是_____________________。
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是_____________________。
(4)一种甲醇燃料电池,使用的电解质溶液是2mol·L-1的KOH溶液。

请写出加入(通入)b物质一极的电极反应式_________________;
每消耗6.4g甲醇转移的电子数为_______________。
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合后,溶液中:2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数Ka为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属钠的叙述中,正确的是( )
A.为防止钠与水反应时燃烧,可将该反应置于试管中进行,以减少与氧气的接触
B.钠着火时应用干燥的沙土灭火
C.钠在空气中受热时,熔化为银白色的小球,产生黄色的火焰,生成白色粉末
D.钠在空气中长期放置,最终主要生成物为过氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是八种环状的烃类物质:

(1)互为同系物的有___________和___________(填序号);互为同分异构体的有___________和___________、___________和___________(填写序号,可以不填满,也可以再补充)。
(2)正四面体烷的二氯取代产物有___________种;立方烷的二氯取代产物有__________种;金刚烷的一氯取代产物有_______________种。
(3)写出两个符合下列条件的物质的结构简式并用系统命名法命名:
a.与苯互为同系物; b.碳原子数小于10;c.一氯代物只有两种。___________________________;___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其淸如水,味极浓烈,盖酒露也。”这里所用的“法”是指
A. 萃取 B. 渗析 C. 蒸馏 D. 过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2—二溴乙烷,用16.0g的溴和足量的乙醇制备1,2—二溴乙烷,实验结束后得到9.4g产品。实验装置如下图所示:

有关数据列表如下:
乙醇 | 1,2—二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度 / g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点 / 0C | 78.5 | 132 | 34.6 |
熔点 / 0C | -130 | 9 | -116 |
溶解性 | 易溶水 | 难溶水 | 微溶于水 |
请回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其主要目的是 (填正确选项前的字母) ;
a、引发反应 b、加快反应速度 c、防止乙醇挥发 d、减少副产物乙醚生成
(2)在装置C中应加入 ,其目的是___________________;(填正确选项前的字母)
a、水 b、浓硫酸 c、氢氧化钠溶液 d、酸性KMnO4溶液
(3)判断该制备反应已经结束的最简单的方法是 。
(4)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在 层(填“上”或“下”);
(5)在装置B中较长玻璃导管的作用是 ;
(6)反应过程中应用冷水冷却装置D,其主要目的是 ,但又不能过度冷却(如用冰水),其原因是 ;
(7)本实验中,1,2—二溴乙烷的产率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com