
丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。已知:
①2C3H8(g) +7O2(g) = 6CO(g)+8H2O(g)?? △H = -2389.8 kJ/mol
②2CO(g) + O2(g) = 2CO2(g)????????????? △H = -566 kJ/mol
③H2O(l) = H2O(g)???? △H = + 44.0 kJ/mol
(1)写出C3H8燃烧时燃烧热的热化学方程式???????????????????????????????????????????? 。
(2)C3H8在不足量的氧气里燃烧,生成CO、CO2、H2O(g),将所有的产物通入一个体积固定的密闭
容器中,在一定条件下发生如下可逆反应: CO(g) +? H2O(g) CO2(g) +? H2(g)
CO2(g) +? H2(g)
该反应的平衡常数与温度的关系如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
保持温度为800℃,在甲、乙两个恒容密闭容器中,起始时按照下表数据进行投料,充分反应直至达到平衡。
| H2O | CO | CO2 | H2 |
甲 (质量/g) | 1.8 | 8.4 | a | 1 |
乙 (质量/g) | 1.8 | 2.8 | 0 | 0 |
①起始时,要使甲容器中反应向正反应方向进行,则a的取值范围是????????????????? ;达到平衡
时,乙容器中CO的转化率为???????? 。
②如图表示上述甲容器中反应在t1时刻达到平衡,在t2时刻因改变某一个条件而发生变化的情况。则t2时刻改变的条件可能是???????????????????????????? 、??????????????????? (答两个要点即可)。

(3)CO2可用NaOH溶液吸收得到Na2CO3或NaHCO3。
① Na2CO3溶液中离子浓度由大到小的顺序为 ?????????? ??? ;
② 已知25℃时,H2CO3的电离平衡常数K1 = 4.4×10-7 mol/L、K2 = 4.7×10-11 mol/L,当Na2CO3溶液的pH为11时, 溶液中c(HCO3-)∶c(CO32-) = ?????????? 。
③ 0.1 mol/L Na2CO3溶液中c(OH-) - c(H+ ) = ?????????????????????? [用含c(HCO3-)、c(H2CO3)的符号表示]。
(1)C3H8(g) +5O2(g) = 3CO2(g)+4H2O(l)?? △H = -2219.9 kJ/mol
(2)① 0 ≤a <2.64??? ;?? 50%???
② 降低温度、降低H2浓度、增大H2O(g)浓度
(3)① c(Na+) > c(CO32-) > c(OH-) > c(HCO3-) > c(H+)
② 1 : 4.7
③ c(HCO3-) + 2c(H2CO3)
【解析】
试题分析:(1)燃烧热是1mol的物质完全燃烧产生稳定的氧化物时所放出热量的化学方程式。将(①+②×3- ③×8)÷2,整理可得:C3H8(g)+5O2(g) =3CO2(g)+4H2O(l)?? △H =-2219.9 kJ/mol。(2)①该反应是个反应前后气体体积相等的反应。在800℃时化学平衡常数为1.对于甲来说,在反应开始时,若CO2的质量为0,则反应一定正向进行,n(H2O)=0.1mol; n(CO)=0.3mol; n(CO2)=a/44mol, n(H2)=0.5mol.)若要使反应正向进行。起始时,则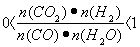 ;
; 。解得0<a<2.64.
。解得0<a<2.64.
对于乙来说:开始时n(H2O)=0.1mol;n(CO)=0.1mol ;n(CO2)=0 ;n(H2)=0;假设在反应的过程中CO转化的物质的量为x,则在平衡时各种物质的物质的量为:n(H2O)=(0.1-x)mol; n(CO)=(0.1-x)mol ; %n(CO2)=xmol;n(H2)=xmol。由于该反应是反应前后气体体积相等的反应,而且在800℃时的平衡常数为1.所以(0.1-x)×(0.1-x)=x2.解得x=0.05mol.所以CO的转化率为0.05÷0.1×100%=50%。②由化学平衡常数以温度的关系可知:升高温度,化学平衡产生减小。说明升高温度,化学平衡向逆反应方向移动。根据平衡移动原理,升高温度,化学平衡向吸热反应方向移动。逆反应方向为吸热反应,所以该反应的正反应为放热反应。由于在平衡后改变某一条件,时,c(CO2)增大,c(CO)减小,所以改变外界条件使平衡正向移动,可以通过降低温度的方法来实现。因为反应前后气体的体积相等,所以改变压强,化学平衡不发生移动。若增大H2O 蒸汽的浓度或减小H2的浓度都会使化学平衡正向移动。因此改变的外界条件是降低温度、降低H2浓度、增大H2O(g)浓度。(3)①Na2CO3是强碱弱酸盐。Na2CO3=2Na++CO32-,CO32-会发生水解反应:CO32-+ H2O HCO3-+ OH-消耗水电离产生的H+,促进水的电离。产生的HCO3-会继续水解:HCO3-+ H2O
HCO3-+ OH-消耗水电离产生的H+,促进水的电离。产生的HCO3-会继续水解:HCO3-+ H2O H2CO3+ OH-。当最终达到平衡时c(OH-)> c(HCO3-) >c(H+) .所以在Na2CO3溶液中离子浓度由大到小的顺序为c(Na+) > c(CO32-) > c(OH-) > c(HCO3-) > c(H+)。②HCO3-
H2CO3+ OH-。当最终达到平衡时c(OH-)> c(HCO3-) >c(H+) .所以在Na2CO3溶液中离子浓度由大到小的顺序为c(Na+) > c(CO32-) > c(OH-) > c(HCO3-) > c(H+)。②HCO3- H++ CO32-
H++ CO32- 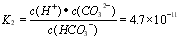 .
.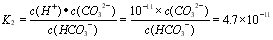 ;
; ;
; 。③Na2CO3溶液显碱性,根据质子守恒可得c(OH-)=c(H+ )(始) = c(H+ )+ c(HCO3-)+2(H2CO3)。所以c(OH-)-c(H+ ) = c(HCO3-)+2(H2CO3)。
。③Na2CO3溶液显碱性,根据质子守恒可得c(OH-)=c(H+ )(始) = c(H+ )+ c(HCO3-)+2(H2CO3)。所以c(OH-)-c(H+ ) = c(HCO3-)+2(H2CO3)。
考点:考查热化学方程式的书写、物质的转化率、平衡移动的措施、离子浓度的大小比较的知识。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com