
(14分)硒34Se和碲52Te都是第VIA族元素,硒是分布在地壳中的稀有元素。工业上用硒鼓废料(主要成分硒、碲、碳、铜和铁合金)回收精炼硒的流程如下:

已知:

(1)Se的氢化物的电子式是____。
(2)步骤①中通人的氧气使硒鼓废料翻腾,目的是 。
(3)废气的主要成分是____ ;废渣II的主要成分是 。
(4)步骤④中主要反应的化学方程式是 ;步骤⑥反应的化学方程式是 。
(5)根据表中数据,步骤⑤最适宜的分离方法是 。
(14分)
(1)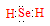
(2)增大接触面积,加快反应速率,使废料充分燃烧
(3)CO2 TeO2
(4)H2SeO3 SeO2+ H2O 2H2SO3+SeO2=Se+2H2SO4
SeO2+ H2O 2H2SO3+SeO2=Se+2H2SO4
(5)升华,将温度控制在315°C到450°C之间
【解析】
试题分析:(1)Se是第六主族元素,氢化物的化学式与H2O相似,属于共价化合物,电子式为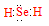 ;
;
(2)步骤①中通人的氧气使硒鼓废料翻腾,目的是增大接触面积,加快反应速率,使废料充分燃烧
(3)根据硒鼓废料的成分判断,废气是CO2;SeO2易溶于水,TeO2微溶于水,所以废渣主要是TeO2;
(4)SeO2溶于水生成H2SeO3,受热分解生成SeO2,化学方程式为H2SeO3 SeO2+H2O;步骤⑥发生氧化还原反应 ,根据所给反应物和产物写出其化学方程式:2H2SeO3+SeO2=Se+2H2SO4
SeO2+H2O;步骤⑥发生氧化还原反应 ,根据所给反应物和产物写出其化学方程式:2H2SeO3+SeO2=Se+2H2SO4
(5)根据SeO2和TeO2升华的温度,二者分离的最适宜方法是升华。
考点:考查Se元素的性质,电子式、化学方程式的书写,物质分离方法的判断


科目:高中化学 来源:2013-2014北京市丰台区高三二模理综化学试卷(解析版) 题型:简答题
(12分)空气吹出法是最早工业化海水提溴的方法,适合从低浓度含溴溶液中提取溴。

(1)NaBr的电子式是 。
(2)反应①是将Br—转化为Br2,反应①的离子方程式是 。
(3)通入空气吹出Br2,并用Na2CO3吸收的目的是 。
(4)反应②的化学方程式是 。
(5)反应③中每生成3 mol Br2,转移电子的物质的量是 mol。
(6)为了除去工业Br2中微量的Cl2,可向工业Br2中 (填字母)。
a.通入HBrb.加入NaBr溶液 c.加入Na2CO3溶液 d.加入Na2SO3溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市丰台区高三二模理综化学试卷(解析版) 题型:选择题
下列叙述中正确的是

A.图①中正极附近溶液pH降低
B.图①中电子由Zn流向Cu,盐桥中的Cl—移向CuSO4溶液
C.图②正极反应是O2+2H2O+4e?  4OH?
4OH?
D.图②中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市东城区高三二模理综化学试卷(解析版) 题型:推断题
(16分)有机物5-甲基茚( )是一种医药合成中间体,某同学设计它的合成路线如下:
)是一种医药合成中间体,某同学设计它的合成路线如下:

已知:i.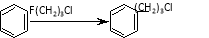
ii.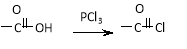
(1)①的反应类型是______。
(2)E的结构简式是______。
(3)A的结构简式是______; ③的反应条件和无机试剂是______。
(4)下列有关5-甲基茚(  )的说法正确的是______(填序号)。
)的说法正确的是______(填序号)。
a. 一定条件下能与卤素单质发生取代反应
b. 1 mol 该物质最多与4 mol H2发生加成反应
c. 一定条件下能发生加聚反应生成高分子化合物
d. 与溴的四氯化碳溶液反应得到的产物不能使高锰酸钾酸性溶液褪色
(5)反应⑧的化学方程式是______。
(6)满足下列条件的G的同分异构体有______种;写出其中一种的结构简式_______。
①分子中含有苯环且苯环上只有一个取代基;②能发生银镜反应。
查看答案和解析>>
科目:高中化学 来源:2013-2014内蒙古鄂尔多斯市高一下学期期末质量检测化学试卷(解析版) 题型:选择题
对于放热反应:H2+Cl2 2HCl,下列说法错误的是
2HCl,下列说法错误的是
A.反应物的总能量大于生成物的总能量
B.该反应遵循“能量守恒定律”
C.该反应中,化学能只转变成热能
D.断开1molH-H键和1molCl-Cl键所吸收的总能量小于形成2molH-Cl键所放出的能量
查看答案和解析>>
科目:高中化学 来源:2013-2014云南省红河州高三下学期毕业生复习统一检测理综化学试卷(解析版) 题型:填空题
(15分)硬质玻璃管是化学实验中经常使用的一种仪器,请分析下列实验(固定装置略)并回答问题。

Ⅰ、进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。请填写表中的空白:
棉球 | 棉球上滴加的试剂 | 实验现象 | 解释和结论 |
a |
| 棉球变白,微热后又恢复红色 |
|
b | 含酚酞的NaOH溶液 | 棉球变为白色 | 离子方程式: |
c |
| 棉球变为白色 | 该气体具有 (选填“氧化性”或“还原性”) |
Ⅱ、硬质玻璃管与其它装置结合完成定性或定量实验。下图是某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究的装置。

实验一:铁矿石中含氧量的测定
(1)按上图组装仪器(夹持仪器均省略),检查装置的气密性;
(2)将10.0g铁矿石放入硬质玻璃管中;
(3)从左端导气管口处不断地缓缓通入H2, 后,点燃A处酒精灯;
(4)充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(5)测得反应后装置B增重2.70g,则铁矿石中氧的质量分数为______________________。
实验二:铁矿石中含铁量的测定

(1)步骤②和⑤中都要用到的玻璃仪器是 __。
(2)下列有关步骤⑥的操作中说法不正确的是_______。
A.滴定管用蒸馏水洗涤后再用待装液润洗
B.锥形瓶需要用待测液润洗
C.因为碘水为黄色,所以滴定过程中不需加指示剂
实验结论:推算铁的氧化物的组成,由实验一、二得出该铁矿石中铁的氧化物的化学式为
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石油裂解可以得到氯乙烯 |
| B.油脂水解可得到氨基酸和甘油 |
| C.所有烷烃和蛋白质中都存在碳碳单键 |
| D.淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com