
| A. | N-H键键能的含义是把1molNH3中的共价键全部拆开所吸收的能量 | |
| B. | ClO-的空间构型为平面三角形 | |
| C. | 卤素单质从F2到I2,在常温常压下的聚集状态由气态、液态到固态的原因是原子半径逐渐增大 | |
| D. | 熔点由高到低的顺序为:金刚石>MgO>NaCl>CCl4 |
分析 A.键能是指生成(或拆开)1mol化学键释放(或吸收)的能量;
B.次氯酸根离子中O原子价层电子对个数是4且含有2个孤电子对,根据价层电子对互斥理论判断空间构型;
C.分子晶体的聚集状态与分子间作用力有关,结构相似的分子晶体相对分子质量越大,分子间作用力越大;
D.一般来说,晶体熔沸点:原子晶体>离子晶体>分子晶体,离子晶体熔沸点与晶格能成正比,晶格能与离子半径成反比,与电荷成正比.
解答 解:A.键能是指生成(或拆开)1mol化学键释放(或吸收)的能量,1mol氨气分子中含有3molN-H键,所以N-H键键能的含义是把NH3中1mol N-H键全部拆开所吸收的能量,故A错误;
B.次氯酸根离子中O原子价层电子对个数是4且含有3个孤电子对,根据价层电子对互斥理论判断空间构型为直线形,故B错误;
C.F2到I2在常温常压下的聚集状态的改变原因是分子间作用力的改变,结构相似的分子晶体相对分子质量越大,分子间作用力越大,所以卤素单质从F2到I2在常温常压下的聚集状态由气态、液态到固态,故C错误;
D.一般来说,晶体熔沸点:原子晶体>离子晶体>分子晶体,离子晶体熔沸点与晶格能成正比,晶格能与离子半径成反比,与电荷成正比,金刚石是原子晶体、MgO和NaCl是离子晶体、四氯化碳是分子晶体,且晶格能MgO>NaCl,所以熔点由高到低的顺序为:金刚石>MgO>NaCl>CCl4,故D正确;
故选D.
点评 本题考查较综合,涉及晶体熔沸点高低判断、分子间作用力、微粒空间构型判断、键能等知识点,侧重考查学生分析判断能力,为高频考点,注意晶格能大小比较方法、微粒空间构型判断方法,题目难度不大.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:多选题
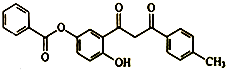
| A. | 分子中含醚键,不含手性碳原子 | |
| B. | 在空气中易被氧化变质 | |
| C. | 能发生取代、加成、消去反应 | |
| D. | 1mol该物质最多能与3mol NaOH溶液发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 碳酸钠溶液中加入足量盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部正确 | B. | 只有①⑤正确 | ||
| C. | 只有③正确 | D. | 以上说法都是错误的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧燃料电池可将热能直接转变为电能 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 燃料电池与干电池或蓄电池的主要差别在于反应物不是储存在电池内部,而是由外设装备提供燃料和氧化剂 | |
| D. | 氢氧燃料电池工作时氢气在正极被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | |
| B. | 硅酸钠溶液与醋酸溶液混合:SiO32-+2H+═H2SiO3↓ | |
| C. | 0.01 mol/L NH4Al(SO4)2溶液与0.02 mol/L Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的氢化物沸点大于Y的氢化物沸点 | |
| B. | Z在Y中燃烧生成的化合物中既含有离子键,又含有共价键 | |
| C. | 原子半径由大到小的顺序:X、Y、Z | |
| D. | 最高价氧化物对应水化物的酸性由强到弱的顺序:W、Y、X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应开始时的速率:甲<乙 | |
| B. | 反应开始时,酸的物质的量浓度:甲>乙 | |
| C. | 反应开始时,酸的物质的量浓度:甲<乙 | |
| D. | 反应所需时间:甲<乙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com