
| A���ɴ˷�Ӧ��֪������K2Cr2O7��Cl2 |
| B���������ͻ�ԭ�������ʵ���֮��Ϊ1:6 |
| C����ת��0.2mol����ʱ�����ɵĻ�ԭ��������ʵ���Ϊ0.1mol |
| D������������ԭ��Ӧ����Ԫ����μӷ�Ӧ����Ԫ�صı�Ϊ3:7 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������ԭ��Ӧ�ı����ǻ��ϼ۵������������ǵ��ӵĵ�ʧ����ӶԵ�ƫ�� | ||||
| B��һ���ָ��ֽⷴӦ������������ԭ��Ӧ | ||||
C���ڷ�Ӧ2H2O
| ||||
| D����������ԭ��Ӧ���������õ����ӷ���������Ӧ����ԭ��ʧȥ���ӷ�����ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
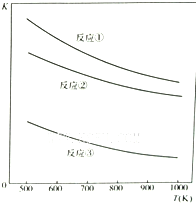
| A����Ӧ�١��ڡ��������������ﶼ�������� |
| B����Ӧ�١��ڡ��۵�����Ӧ���Ƿ��ȷ�Ӧ |
| C����Ӧ�١��ڡ����У��¶�Խ��H2S���ѳ���Խ�� |
| D����Ӧ�١��ڡ����У�ѹǿԽ��H2S�ѳ���Խ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1��10 | B��1��8 | C��1��5 | D��1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ||
| A���٢� | B���٢� | C���ڢ� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.3mol.L-1 | B��0.225mol.L-1 | C��0.15mol.L-1 | D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
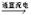 Cl2��+H2��+2NaOH��
Cl2��+H2��+2NaOH��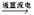 Cl2��+ Cu d��3Cl2 + 2Fe
Cl2��+ Cu d��3Cl2 + 2Fe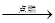 2FeCl3
2FeCl3�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����


| A�������ڿ�����������ַ�Ӧ | B����ȥ�����е�ˮ���� |
| C�������������� | D�������ڹ۲�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��SO2ֻ���������� |
| B��CuFeS2������ԭ������Ԫ�ر����� |
| C��ÿ����1molCu2S����4mol������ |
| D��ÿת��1.2mol���ӣ���0.2mol������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com