
(2013?辽宁一模)[化学--选修3物质结构与性质]
已知R、W、X、Y、Z是周期表中前四凰期元素,它们的原子序数依次递增.R的基态原子中占据哑铃形原子轨道的电子数为1;W的氢化物的沸点比同族其它元素氢化物的沸点高;X
2+与W
2-具有相同的电子层结构;Y元素原子的3p能级处于半充满状态;Z
+的电子层都充满电子.请回答下列问题:
(1)写出Z的基态原子的外围电子排布式
3d104s1
3d104s1
.
(2)R的某种钠盐晶体,其阴离子A
m-(含R、W、氢三种元素)的球棍模型如图所示:在A
m-中,R原子轨道杂化类型有
SP2、SP3
SP2、SP3
;m=
2
2
.(填数字)
(3)经X射线探明,X与W形成化合物的晶体结构与NaCl的晶体结构相似,X
2+的配位原子所构成的立体几何构型为
正八面体
正八面体
.
(4)往Z的硫酸盐溶液中加入过量氨水,可生成[Z(NH
3)
4]SO
4,下列说法正确的是
AD
AD
A.[Z(NH
3)
4]SO
4中所含的化学键有离子键、极性键和配位键
B.在[Z(NH
3)
4]SO
4中Z
2+给出孤对电子,NH
3提供空轨道
C.[Z(NH
3)
4]SO
4组成元素中第一电离能最大的是氧元素
D.SO
42-与PO
43-互为等电子体,空间构型均为四面体
(5)固体YCl
5的结构实际上是Ycl
4+和YCl
6-构成的离子晶体,其晶体结构与CsCl相似.若晶胞边长为apm,则晶胞的密度为
g?cm
-3.

 (2013?辽宁一模)[化学--选修3物质结构与性质]
(2013?辽宁一模)[化学--选修3物质结构与性质]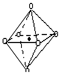 ,故配位原子所构成的立体几何构型为正八面体,
,故配位原子所构成的立体几何构型为正八面体,
