
 ,则该有机物核磁共振氢谱有3个峰.
,则该有机物核磁共振氢谱有3个峰.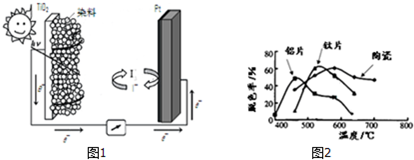
分析 (1)TiCl4水解生成二氧化钛和氯化氢;
(2)氯气具有强氧化性,可与KI反应生成碘单质,淀粉遇碘变蓝色;分子中有几种氢,核磁共振氢谱有几种峰;
(3)由图电子的移动方向可知,半导材料TiO2与染料为原电池的负极,铂电极为原电池的正极,电解质为I3-和I-的混合物,I3-在正极上得电子被还原;
(4)根据图中脱色率与温度关系解题.
解答 解:(1)高温条件下,TiCl4水解生成二氧化钛和氯化氢,化学反应式为TiCl4+2H2O$\frac{\underline{\;高温\;}}{\;}$TiO2+4HCl,
故答案为:TiCl4+2H2O$\frac{\underline{\;高温\;}}{\;}$TiO2+4HCl;
(2)氯气具有强氧化性,可与KI反应生成碘单质,淀粉遇碘变蓝色,所以可将湿润的淀粉KI试纸置于集气瓶口,证明有氯气;分子中有3种氢,核磁共振氢谱有3个峰,
故答案为:用湿润的KI-淀粉试纸检验;3;
(3)由图电子的移动方向可知,半导材料TiO2与染料为原电池的负极,铂电极为原电池的正极,电解质为I3-和I-的混合物,I3-在正极上得电子被还原,正极反应为I3-+2e-=3I-,
故答案为:I3-+2e-=3I-;
(4)a.由图知,500度以下钛片最差,故a错误;
b.由图知,在520℃时,脱色率最高,钛片载体的光催化活性最好,故b正确;
c.520℃后钛片催化活性随温度的升高而较低,故c错误;
d.由图知,相同温度时,不同的载体(钛片、铝片、陶瓷),TiO2薄膜的光催化活性不同,故d正确.
故答案为:bd.
点评 本题考查原电池的工作原理、物质的检验、元素化合物的性质等,题目难度不大,本题注意把握电极反应式的书写,图中电子的移动方向是解答的关键,侧重于考查学生对基础知识的综合应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 将40gNaOH溶解于1L水中 | |
| B. | 将22.4L氯化氢气体溶于水配成1L溶液 | |
| C. | 将1L10mol/L的浓盐酸与9L水混合 | |
| D. | 将10gNaOH溶解于水中配成250mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl | B. | 金刚石和石墨 | ||
| C. | 乙烷和丙烷 | D. | T2O和D2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液与盐酸中和 | B. | 分解氯酸钾制氧气 | ||
| C. | Zn与CuSO4 溶液的反应 | D. | MgCl2溶液与KOH溶液产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10℃时,块状锌与3 mol/L硫酸溶液反应 | |
| B. | 30℃时,粉末状锌与3 mol/L硫酸溶液反应 | |
| C. | 10℃时,粉末状锌与3 mol/L硫酸溶液反应 | |
| D. | 30℃时,块状锌与3 mol/L硫酸溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com