
��һ�������£���һ�ݻ��ɱ���ܱ������У���SO2��O2��Ϸ�����Ӧ��
2SO2(g)��O2(g) 2SO3(g)��Q
2SO3(g)��Q
��Ӧ�����У�SO2��O2��SO3�����ʵ���(mol)�ı仯���±���

�ش��������⣺
(1)��Ӧ����ƽ��״̬��ʱ��Ϊ________��
(2)SO3(g)��һ�������·ֽ�����SO2��O2(g)�ﵽƽ�⣬д���˷�Ӧ��ƽ�ⳣ���ı���ʽK________��
(3)��4��5 minʱ����������ʵ����仯��ԭ����________��ƽ����________�����ƶ���
(4)��0.1 Mpa��500��ʱ����Ӧ��ʼʱO2��SO2�����ʵ���֮��![]() ��ֵ����ƽ��ʱSO2������ٷֺ�����ϵ�ı仯������ͼ��ʾ��
��ֵ����ƽ��ʱSO2������ٷֺ�����ϵ�ı仯������ͼ��ʾ��
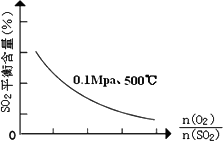
��ͼ�л�������ͬѹǿ�£��¶�Ϊ400��ʱ����Ӧ��ʼʱO2��SO2�����ʵ���֮��![]() ��ֵ����ƽ��ʱSO2������ٷֺ�����ϵ�Ĵ��±仯���ߣ�
��ֵ����ƽ��ʱSO2������ٷֺ�����ϵ�Ĵ��±仯���ߣ�
 ��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 �����йط�Ӧ���£�
�����йط�Ӧ���£�| c2(NO2) |
| C2(NO)c(O2) |
| c2(NO2) |
| C2(NO)c(O2) |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
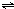 ClO��g��+3H2��g����H��0��
ClO��g��+3H2��g����H��0��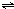 CH3OH��g����H=-90.1kJ?mol-1�����������´�ƽ�⣬���д�ʩ����ʹn��CH3OH��/n��CO���������
CH3OH��g����H=-90.1kJ?mol-1�����������´�ƽ�⣬���д�ʩ����ʹn��CH3OH��/n��CO���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 3C��������һ�������£���һ�ܱա����ݵ������У�ʹһ����A��B���巴Ӧ�����������������жϴﵽƽ��״̬���ǣ�������
3C��������һ�������£���һ�ܱա����ݵ������У�ʹһ����A��B���巴Ӧ�����������������жϴﵽƽ��״̬���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
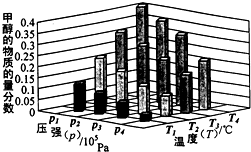 ��Դ����Լ���ҷ�չ���̵�����֮һ���״��������ѵȱ���Ϊ2 1���͵���ɫ��Դ����ҵ��������Ȼ��Ϊ��Ҫԭ���������̼��ˮ������һ���������Ʊ��ϳ�����CO��H2�������Ƴɼ״��������ѣ�
��Դ����Լ���ҷ�չ���̵�����֮һ���״��������ѵȱ���Ϊ2 1���͵���ɫ��Դ����ҵ��������Ȼ��Ϊ��Ҫԭ���������̼��ˮ������һ���������Ʊ��ϳ�����CO��H2�������Ƴɼ״��������ѣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�״���ͨ����ú���������������ɵ�CO��H2��һ�������·������·�Ӧ�Ƶã�CO(g) + 2H2(g)��CH3OH(g)
�������ͼ�ش��������⣺
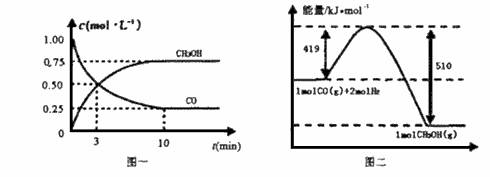
(1)�ӷ�Ӧ��ʼ��ƽ�⣬��COŨ�ȱ仯��ʾƽ����Ӧ����v(CO)�� ��
(2)д���÷�Ӧ���Ȼ�ѧ����ʽ ��
n(CH3OH)
(3)���������£����д�ʩ����ʹ n(CO) ������� ��
A.�����¶� B.����He�� C.�ٳ���1 mol CO��2 mol H2 D.ʹ�ô���
(4)�����¶Ⱥ��ݻ���ͬ�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���÷�Ӧ�ﵽƽ��ʱ���й��������±���
| ���� | ��Ӧ��Ͷ����� | ��Ӧ���ת���� | CH3OH��Ũ�� | �����仯��Q1��Q2��Q3������0�� |
| �� | 1 mol CO��2 mol H2 | a1 | c1 | �ų�Q1kJ���� |
| �� | 1 mol CH3OH | a2 | c2 | �ų�Q2kJ���� |
| �� | 2mol CO��4 mol H2 | a3 | c3 | �ų�Q3kJ���� |
�����й�ϵ��ȷ���ǣ�
A. c1��c2 B.2Q1��Q3 ���� C.2a1��a3 D. a1+ a3��1
E.�÷�Ӧ������1 mol CH3OH����ų���Q1+ Q2��kJ����
(5)����һ����ɱ���ܱ������г���1 mol CO��2 mol H2��1 mol CH3OH���ﵽƽ��ʱ��û��������ܶ���ͬ��ͬѹ����ʼ��1.6������÷�Ӧ�� ������������桱����Ӧ�����ƶ���������
��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com