
A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.
(1)W2-离子的结构示意图为 ,E元素在周期表中的位置为 ,写出E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式 。
(2)经测定A2W2为二元弱酸,A2W2的电子式为 ,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式 。
(3)向含有Fe2+和淀粉KI的酸性溶液中滴入A2W2,观察到溶液呈蓝色并有红褐色沉淀成.当消耗2mol I﹣时,共转移3mol电子,该反应的离子方程式是 。
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,写出该反应方程式 ,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是 L(标准状况下)。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017陕西西安长安区一中重点班高一12月考化学卷(解析版) 题型:选择题
将一小块金属钠长期露置于空气中 发生一系列变化,最终产物是 ( )
发生一系列变化,最终产物是 ( )
A、Na2O B、Na2O2 C、NaOH D、Na2CO3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
下列各组离子在指定溶液中一定能大量共存的是( )
①pH = 0的溶液:Na+、Cl—、MnO4—、SO42—
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32-
③水电离的H+浓度c(H+)=10-12mol·L-1的溶液中:Cl-、CO32-、NO3-、NH4+、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
⑤使石蕊变红的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、I-、Cl-、S2-
A.②④ B.①③⑥ C.①②⑤ D.①②④
查看答案和解析>>
科目:高中化学 来源:2017届安徽马鞍山二中安师大附中高三12月联考化学卷(解析版) 题型:填空题
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度。
(1)若将W g Na2C2O4配成100mL标准溶液,移取20.00mL置于锥形瓶中,则酸性KMnO4溶液应装在______(填“酸式”或“碱式”)滴定管中,判断滴定达到终点的现象是_________________。
(2)写出KMnO4与热的经硫酸酸化的Na2C2O4反应生成Mn2+和CO2的化学方程式:________________________。
(3)25℃时,用pH计测得0.10 mol·L-1草酸钠溶液的pH=a,则H2C2O4的第二级电离平衡常数Ka2= 。
(4)CaC2O4是难溶于水的固体,受热易分解,在一定温度下向2L的密闭容器放入足量草酸钙(固体所占体积忽略不计)发生反应: CaC2O4(s) CaO(s)+CO(g)+CO2(g),若前5min内生成CaO的质量为16.8g,则该段时间内υ(CO)=__________mol·L-1·s-1;当反应达到平衡后,将容器体积压缩到原来的一半,则下列说法正确的是__________(填答案选项编号)。
CaO(s)+CO(g)+CO2(g),若前5min内生成CaO的质量为16.8g,则该段时间内υ(CO)=__________mol·L-1·s-1;当反应达到平衡后,将容器体积压缩到原来的一半,则下列说法正确的是__________(填答案选项编号)。
A.平衡不移动,CaO的质量不变
B.平衡发生移动,当CO的百分含量不变时达到新的平衡
C.平衡发生移动,但CO和CO2的浓度都没有改变
D.平衡向逆反应方向移动,且该反应的化学平衡常数减小
查看答案和解析>>
科目:高中化学 来源:2017届安徽马鞍山二中安师大附中高三12月联考化学卷(解析版) 题型:选择题
如图所示有机物的一氯取代物有(不含立体异构)( )
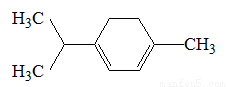
A.5种 B.6种 C.7种 D.8种
查看答案和解析>>
科目:高中化学 来源:2017届重庆市西北狼教育联盟高三12月月考化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论不正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 向某溶液中加入盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 该溶液中不一定含有SO42﹣ |
B | FeCl2溶液中,滴加KSCN溶液和溴水 | 滴加KSCN溶液,无明显变化;滴加溴水后,溶液变红 | 氧化性:Br2>Fe3+ |
C | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
D | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al |
查看答案和解析>>
科目:高中化学 来源:2017届江苏省淮安市高三12月考试化学试卷(解析版) 题型:填空题
[物质结构与性质]
亚硝酸盐与钴(Ⅲ)形成的一种配合物1Co(NH3)5NO2]Cl2的制备流程如下:
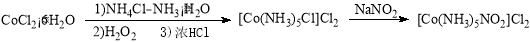
(1)Co2+基态核外电子排布式为 。
(2)配合物1Co(NH3)5Cl]Cl2中与Co3+形成配位键的原子为 (填元素符号);配离子 1Co(NH3)5NO2]2+的配体中氮原子的杂化轨道类型为 。
(3)与NO2-互为等电子体的单质分子为 (写化学式)。
(4)H2O2与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为 。
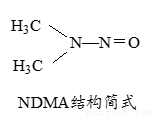
(5)亚硝酸盐在水体中可转化为强致癌物亚硝胺,亚硝胺NDMA的结构简式如图所示,1molNDMA分子中含有σ键的数目为 mol。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省淮安市高三12月考试化学试卷(解析版) 题型:选择题
下列有关物质的性质与用途具有对应关系的是
A.SO2具有还原性,可用于漂白纸浆
B.NH4HCO3受热易分解,可用作氮肥
C.氢 氧化铝具有弱碱性,可用作净水剂
氧化铝具有弱碱性,可用作净水剂
D.常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上模拟四化学试卷(解析版) 题型:推断题
根据下列框图回答问题(答题时方程式中的M、E用所对应的元素符号表示):
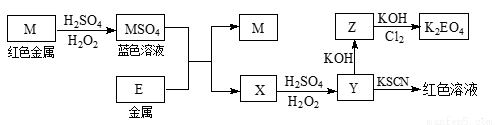
(1)写出M、E的化学式:M ;E ;
(2)M溶于稀H2SO4和H2O2混合液的化学方程式: ,若参加反应H2O2为1mol,转移电子为 mol。
(3)某同学取X的溶液,用稀硫酸酸化并在空气中放置一段时间后,加入KI—淀粉溶液,溶液变为蓝色。写出与上述变化过程相关的离子方程式: 、 。
(4)写出Cl2将Z氧化为K2EO4的化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com