
分析 若甲和丙都是不溶于水的白色固体物质,既能溶于盐酸又能溶于氢氧化钠溶液,说明甲和丙是两性物质,结合转化关系可知,甲为Al2O3,氧化铝与硫酸反应生成乙为硫酸铝,硫酸铝与氨水反应生成丙为氢氧化铝,氢氧化铝受热分解得甲为氧化铝,符合各物质的转化关系,据此答题.
解答 解:若甲和丙都是不溶于水的白色固体物质,既能溶于盐酸又能溶于氢氧化钠溶液,说明甲和丙是两性物质,结合转化关系可知,甲为Al2O3,氧化铝与硫酸反应生成乙为硫酸铝,硫酸铝与氨水反应生成丙为氢氧化铝,氢氧化铝受热分解得甲为氧化铝,符合各物质的转化关系,
(1)根据上面的分析可知,甲是 Al2O3,丙是氢氧化铝,化学式为Al(OH)3,
故答案为:Al2O3;Al(OH)3;
(2)乙为硫酸铝,丙是氢氧化铝,“乙$\stackrel{NH_{3}.H_{2}O}{→}$丙”转化的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
点评 本题考查了无机推断,涉及Al元素化合物性质与转化关系,比较基础,注意基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 22 mL、12 mL | B. | 13 mL、21 mL | C. | 16 mL、16 mL | D. | 21 mL、13 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.15 mol/L | B. | 0.3 mol/L | C. | 0.45 mol/L | D. | 0.2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
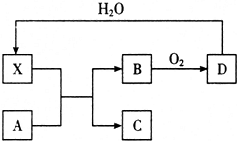 已知X为一种常见酸的浓溶液,能使蔗糖变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物已略去,下列有关说法正确的是( )
已知X为一种常见酸的浓溶液,能使蔗糖变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物已略去,下列有关说法正确的是( )| A. | X能使蔗糖变黑主要体现了 X的强氧化性 | |
| B. | 若A为铁,则足量A与X在室温下即可完全反应 | |
| C. | 若A为碳单质,则将C通入少量澄清石灰水中,最终一定有白色沉淀产生 | |
| D. | 工业上,B转化为D的反应需使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{22.4bc}{a}$NAL | B. | $\frac{22.4ab}{c}$NAL | C. | $\frac{22.4ac}{b}$NAL | D. | $\frac{22.4b}{ac}$NA L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学是在原子、分子水平上研究物质的组成、结构、性质、制备等的自然科学 | |
| B. | 化学是一门具有创造性的科学,可以利用化学知识创造出自然界中不存在的物质 | |
| C. | 化学的发展经过了从宏观到微观,从感性到理性的逐步深化的过程 | |
| D. | 随着化学的发展,人们最终会实现通过化学变化使水变油的梦想 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧瓶、锥形瓶、蒸发皿加热时均需要垫上石棉网 | |
| B. | 分液漏斗、滴定管、容量瓶使用前均需要检查是否漏水 | |
| C. | 配制1 mol•L-1NaCl溶液、测定Na2CO3溶液的pH、焰色反应实验均需要用到玻璃棒 | |
| D. | 乙酸乙酯、硝基苯的制备、银镜反应实验均需要水浴加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com