
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 只含有离子键的化合物才是离子化合物 | |
| C. | 并非只有非金属原子间才能形成共价键 | |
| D. | 由共价键形成的分子一定是共价化合物 |
分析 A.离子化合物中含有离子键,可能含有共价键,只含共价键的化合物是共价化合物;
B.离子化合物中可能含有共价键;
C.并非只有非金属原子间才能形成共价键,金属和非金属元素之间可能形成共价键;
D.由共价键形成的分子可能是单质.
解答 解:A.离子化合物中含有离子键,可能含有共价键,只含共价键的化合物是共价化合物,所以含有共价键的化合物可能是离子化合物,如KOH等,故A错误;
B.离子化合物中可能含有共价键,如Na2O2、含氧酸盐等,故B错误;
C.并非只有非金属原子间才能形成共价键,金属和非金属元素之间可能形成共价键,如氯化铝,故C正确;
D.由共价键形成的分子可能是单质,如氧气等,故D错误;
故选C.
点评 本题考查物质和化学键的关系,为高频考点,明确物质构成微粒及化合物类型判断方法是解本题关键,注意不能根据是否含有金属元素判断离子键,易错选项是C.


科目:高中化学 来源: 题型:选择题
| A. | 3.5×10-3 g | B. | 7×10-4 g | C. | 4.52×10-3 g | D. | 4.52×10-2 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | a的取值范围 | 产物的化学式或(离子符号) |
| A | a≤$\frac{1}{6}$ | I2,Br- |
| B | $\frac{1}{6}$<a<$\frac{1}{5}$ | I2、Br-、Br2 |
| C | a=$\frac{1}{5}$ | I2、Br2 |
| D | $\frac{1}{5}$<a<$\frac{6}{5}$ | I2,IO3-,Br2 |
| E | a≥$\frac{6}{5}$ | IO3-、Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
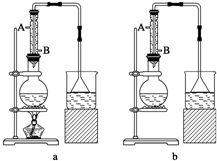
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若烃中碳、氢元素的质量分数相同,则为同系物 | |
| B. | CH2═CH2和CH2═CH-CH═CH2互为同系物 | |
| C. | 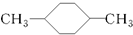 和 和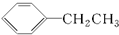 互为同分异构体 互为同分异构体 | |
| D. | 同分异构体的化学性质可能相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 | B. | 0.3 mol•L-1 | C. | 0.5 mol•L-1 | D. | 0.15 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学平衡常数K=$\frac{{c}^{4}(C)•{c}^{2}(D)}{{c}^{3}(A)•{c}^{2}(B)}$ | |
| B. | 增大压强,平衡右移,K平衡增大 | |
| C. | B的平衡转化率是40% | |
| D. | 其他条件不变,向平衡体系中加入少量C,v正、v逆均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫能漂白某些物质,说明它具有氧化性 | |
| B. | 二氧化硫的水溶液能使紫色石蕊试液变红,说明它能与水反应生成H2SO3 | |
| C. | 将足量二氧化硫通入酸性高锰酸钾溶液中,溶液褪色,说明二氧化硫具有还原性 | |
| D. | 将等体积的SO2和Cl2混和后通入滴有石蕊的水中,溶液的颜色将变红 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com