
| A. | 常温下用NaOH溶液吸收Cl2 | B. | Na在空气中燃烧 | ||
| C. | Na2O2吸收CO2 | D. | S在空气中燃烧 |
分析 A.Cl2+2NaOH=NaClO+NaCl+H2O,氯气即是氧化剂又是还原剂;
B.O2+2Na$\frac{\underline{\;点燃\;}}{\;}$Na2O2,钠为还原剂,氧气为氧化剂;
C.2Na2O2+2CO2=2Na2CO3+CO2,Na2O2为还原剂,Na2O2为氧化剂;
D.O2+S$\frac{\underline{\;点燃\;}}{\;}$SO2,S为还原剂,氧气为氧化剂.
解答 解:A.Cl2+2NaOH=NaClO+NaCl+H2O,氯气即是氧化剂又是还原剂,还原剂与氧化剂的质量比和物质的量之比均为1:1,故A不选;
B.O2+2Na$\frac{\underline{\;点燃\;}}{\;}$Na2O2,钠为还原剂,氧气为氧化剂,还原剂与氧化剂的质量比为23:16,还原剂与氧化剂的物质的量之比为2:1,故B选;
C.2Na2O2+2CO2=2Na2CO3+CO2,Na2O2为还原剂,Na2O2为氧化剂,还原剂与氧化剂的质量比和物质的量之比均为1:1,故C不选;
D.O2+S$\frac{\underline{\;点燃\;}}{\;}$SO2,S为还原剂,氧气为氧化剂,还原剂与氧化剂的质量比和物质的量之比均为1:1,故D不选.
故选B.
点评 本题考查氧化还原反应,把握发生的反应及反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:选择题
| A. | 35.7g | B. | 30g | C. | 17g | D. | 9g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度升高,c(HCO3-)减小 | |
| B. | 25℃时,加水稀释后,n(H+)与n(OH-)的乘积变小 | |
| C. | 溶质的电离方程式为NaHCO3═Na++H++CO32- | |
| D. | 离子浓度关系:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铜有毒 | B. | 硫酸铜溶液是蓝色的胶体 | ||
| C. | 硫酸铜为电解质 | D. | 解毒的原因是Cu2+转化为沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解、过滤、蒸发、洗涤 | B. | 溶解、蒸发、洗涤、过滤 | ||
| C. | 溶解、过滤、洗涤、干燥 | D. | 溶解、洗涤、过滤、干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
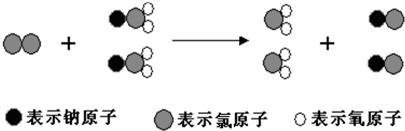
| A. | 该反应的化学方程式为Cl2+2NaClO2═2ClO2+2NaCl | |
| B. | 该反应是应是复分解反应 | |
| C. | 反应中Cl2既是氧化剂,又是还原剂 | |
| D. | NaClO2和ClO2中Cl元素的化合价相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
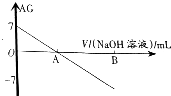 若用AG表示溶液的酸度(acidity grade),AG的定义为AG=lg[$\frac{c({H}^{+})}{c(O{H}^{-})}$].室温下实验室中用0.01mol•L-1的氢氧化钠溶液滴定20.00mL0.01mol•L-1的醋酸,滴定过程如图所示,下列叙述正确的是( )
若用AG表示溶液的酸度(acidity grade),AG的定义为AG=lg[$\frac{c({H}^{+})}{c(O{H}^{-})}$].室温下实验室中用0.01mol•L-1的氢氧化钠溶液滴定20.00mL0.01mol•L-1的醋酸,滴定过程如图所示,下列叙述正确的是( )| A. | 室温下,醋酸的电离常数约为10-5 | |
| B. | A点时加入氢氧化钠溶液的体积为20.00mL | |
| C. | 若B点为40mL,所得溶液中:c(H+)=c(CH3COO-)+c(CH3COOH) | |
| D. | 反应过程中一定存在:0.01mol•L-1+c(OH-)=c(Na+)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量都为4.4g的CH3CHO和CO2含有的分子数均为0.1NA | |
| B. | 1molNa2O2中的离子总数为4NA | |
| C. | 密闭容器中,2molSO2和足量的O2反应转移的电子数为4NA | |
| D. | 1mol苯分子中所含的碳碳双键数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com