
将17.9 g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体3.36 L(标准状况)。另取等质量的合金溶于过量的稀硝酸中,生成6.72 L NO(标准状况),向反应后的溶液中加人过量NaOH溶液,得到沉淀的质量为
A.33.2 g B.25.4 g C.22.4 g D.19.6 g
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案科目:高中化学 来源:2016届四川省高三上学期10月月考化学试卷(解析版) 题型:填空题
亚硫酸钠(Na2SO3)、漂白液(NaClO)和明矾[KAl(SO4)2?12H2O]都是重要的化工产品,在日常生活和工业生产中都有广泛用途,且三者都可用在造纸业的不同生产工序中。
(1)NaClO做消毒液是它能与水反应产生一种强氧化性物质,写出该强氧化性物质的电子式_______。在工业上,用氯化钠为原料,在碱性溶液中,通过电解的方法可制得NaClO,用离子方程式表示制取NaClO的电解总反应:____________。将等浓度等体积的NaClO与Na2SO3溶液混合后,两者恰好完全反应,写出混合过程的离子反应方程式 ____________。
(2)将饱和NaClO和KAl(SO4)2溶液混合,置于一只带单孔橡皮塞的大试管中,产生大量的白色胶状沉淀。此时反应的离子方程为____________。再将大试管置于阳光下照射,不久试管液面上方有浅黄绿色气体产生,将气体通入NaOH溶液充分吸收后,还能收集到一种无色无味的气体。写出在阳光照射下,混合液中反应的化学方程式____________。若将KAl(SO4)2溶液换成硫酸亚铁铵【(NH4)2SO4?FeSO4】溶液后,再与NaClO溶液混合,观察试管中有红褐色沉淀产生,同时溶液里现黄色,但没有气体生成。此时试管中发生反应的离子方程式为____________。
(3)取一定体积KAl(SO4)2溶液于试管中,逐滴加入一定浓度的Ba(OH)2溶液, 直至产生沉淀的质量最大,写出此时的离子反应方程式____________。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:填空题
[物质结构与性质]下列反应曾用于检测司机是否酒后驾驶:
2Cr2O72-+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
(1)Cr3+基态核外电子排布式为_______ __;配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是________(填元素符号)。
(2)CH3COOH中C原子轨道杂化类型为___________;1molCH3COOH分子中含有δ键的数目为 _____ _。
(3)与H2O互为等电子体的一种阳离子为_____ ___(填化学式);H2O与CH3CH3OH可以任意比例互溶,除因为它们都是极性分子外,还因为_____ ___。
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三上学期10月月考理综化学试卷(解析版) 题型:选择题
PbO2受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1 mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为1:1,则剩余固体的组成及物质的量比可能是
A.1:2:1混合的PbO2、Pb3O4、PbO
B.1:3:2混合的PbO2、Pb3O4、PbO
C.1:1:1混合的PbO2、Pb3O4、PbO
D.2:1:1混合的PbO2、Pb3O4、PbO
查看答案和解析>>
科目:高中化学 来源:2016届浙江省瑞安市四校高三上学期第一次联考化学试卷(解析版) 题型:选择题
由铝屑、盐酸、氢氧化钠溶液反应制取1mol Al(OH)3,至少需要消耗HCl和NaOH的物质的量为
A.0.25mol,0.25mol B.0.75mol,0.75mol
C.1mol,1mol D.3mol,3mol
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.用到金属钠时,要用镊子取、再用小刀切下所需量,剩余的钠不能放回原试剂瓶中
B.大型中央空调的制冷剂可用液氨
C.常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体
D.测氯水的pH,可用玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较
查看答案和解析>>
科目:高中化学 来源:2016届湖南省益阳市高三上学期第三次模拟化学试卷(解析版) 题型:选择题
用碳棒电极电解一定质量的某浓度的氯化钾溶液,一段时间后停止电解。此时若加入100g 36.5%的浓盐酸,所得溶液正好与原溶液完全相同,则电解过程中转移电子的物质的量约为
A.9 mol B.7 mol C.6 mol D.8 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省泰州市姜堰区高二上学期期中选修化学试卷(解析版) 题型:填空题
白云石的主要成份是CaCO3·MgCO3,在我国有大量的分布。以白云石为原料生产的钙镁系列产品有广泛的用途。白云石经煅烧、熔化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离。
已知:碳化反应是放热反应,化学方程式Ca(OH)2+Mg(OH)2+3CO2 CaCO3+Mg(HCO3)2+H2O。完成下列填空:
CaCO3+Mg(HCO3)2+H2O。完成下列填空:
(1)Ca(OH)2的碱性比Mg(OH)2的碱性 (填“强”或“弱”)
Ca(OH)2的溶解度比Mg(OH)2的溶解度 (填“大”或“小”)。
(2)碳化温度保持在50~60 ℃。温度偏高不利于碳化反应,原因是 、 (至少写2点)。温度偏低也不利于碳化反应,原因是 。
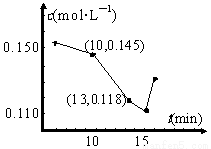
(3)已知某次碳化时溶液中钙离子浓度随时间的变化如图所示,在10 min到13 min之内钙离子的反应速率为 。用化学方程式表示15 min之后钙离子浓度增大的原因 。
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰市宁城县高三上学期第一次统考化学试卷(解析版) 题型:选择题
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S。下列说法不正确的是
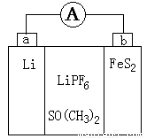
A.可以用水代替SO(CH3)2做溶剂
B.电子移动方向是由a极流向b极
C.该装置将化学能转化为电能
D.b极反应式是FeS2+4Li++4e-=Fe+2Li2S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com