

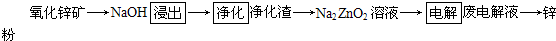
| ��+�� |
| 2 |
| (a+b) |
| 2 |
| (a+b) |
| 2 |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||
| ||

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��Ӧ����ʱ��/min | CO | Zn | CO2 |
| 0 | 0.11 | 0 | 0 |
| 2 | 0.1 | 0.01 | 0.01 |
| 30 | c1 | C2 | C2 |
| 35 | c1 | C2 | C2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011����������һ�и�����ѧ�ڵ�����¿������ۣ���ѧ���� ���ͣ�ʵ����
�ִ���п�ķ����ɷ�Ϊ��ʪ�������࣬������������п�ĸ���Ʒ�����ڸ߶��Խ������Իش������������.
����п�ǽ���п����Ҫ��ZnS��ͨ����ѡ������ʹ��ת��Ϊ����п���ٰ�����п�ͽ�̿��ϣ��ڹķ�¯�м�����1373-1573K��ʹп�����������Ҫ��ӦΪ��
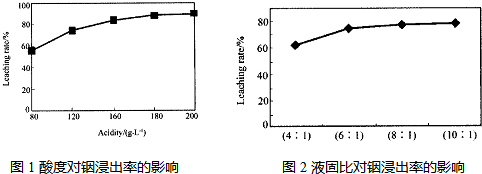
�ӻ���п�����IJ����к����ֽ������ʼ�In2O3������������ȡ����ij�о������Դ��о��������¡�ʵ�����漰����ȣ�ÿ����Һ�к�����������������Ľ���������ͼ1��������Һ������������������ͼ2
ͼ1��ȶ��������ʵ�Ӱ�� ͼ2Һ�̱ȶ��������ʵ�Ӱ��
�ٵ����Ϊ196ʱ�������ʵ���Ũ��Ϊ ��
�ڴӽ�Լԭ�Ϻͽ����ʿ��ǣ����˵���Ⱥ�Һ�̱ȷֱ�Ϊ��_______��_______��
��2��ʪ����п����Ҫ��������Ϊ��
�ٴӱ��������ͳ������ԭ�ϽǶȣ���δ������������� ��
�ڳ�ȥ�����Һ�е���������H2O2�������ٵ���pHʹ֮�γ�Fe(OH)3������д��H2O2����Fe2+�����ӷ���ʽ
�������Һ������Cd2+,Ϊ�˷�ֹ����Ⱦ�������ӣ������������ʵIJ��죬��������������Һ���룬��֪Zn(OH)2����������һ��Ҳ�������ԣ���д����������ӷ���ʽ____________________��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ2010������꼶��һ��ģ�⿼�Ի�ѧ���� ���ͣ������
��8�֣��ִ���п�ķ����ɷ�Ϊ��ʪ�������࣬������������п�ĸ���Ʒ�����ڸ߶��Խ������Իش������������.
��1������п�ǽ���п����Ҫ��ZnS��ͨ����ѡ������ʹ��ת��Ϊ����п���ٰ�����п�ͽ�̿��ϣ��ڹķ�¯�м�����1373-1573K��ʹп���������
��Ҫ��ӦΪ��2ZnS +3O2 2ZnO+2SO2
���ķ�¯�У�2C +O2
2ZnO+2SO2
���ķ�¯�У�2C +O2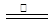 2CO
2CO
�ķ�¯�У�ZnO+CO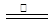 Zn
+ CO2
Zn
+ CO2
�ӻ���п�����IJ����к����ֽ������ʼ�In2O3������������ȡ����ij�о�������Щ�о��������¡�ʵ�����漰����ȣ�ÿ����Һ�к�����������������Ľ���������ͼ1��������Һ������������������ͼ2��

�ٵ����Ϊ196ʱ�������ʵ���Ũ��Ϊ �� ��
�ڴӽ�Լԭ�Ϻͽ����ʿ��ǣ����˵���Ⱥ�Һ�̱ȷֱ�Ϊ�� �� �� �� ��
��2��ʪ����п����Ҫ��������Ϊ��

�������ȡ����Ҫ��Ӧ�����ӷ���ʽΪ�� �� ��
�ڴӱ��������ͳ������ԭ�ϽǶȣ���δ������������� �� ��
�۳�ȥ�����Һ�е���������H2O2�������ٵ���pHʹ֮�γ�Fe(OH)3������д��H2O2����Fe2+�����ӷ���ʽ �� ��
�������Һ������Cd2+,Ϊ�˷�ֹ����Ⱦ�������ӣ������������ʵIJ��죬��������������Һ���룬��֪Zn(OH)2����������һ��Ҳ�������ԣ���д����������ӷ���ʽ �� �� �� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com