
下列组合中,属于含有极性键的非极性分子的是( )
|
| A. | C2H4、C2H2、CO2 | B. | CH4、CHCl3、CO2 |
|
| C. | Cl2、H2、N2 | D. | NH3、H2O、SO2 |
考点:
极性键和非极性键;极性分子和非极性分子.
专题:
化学键与晶体结构.
分析:
同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性键,由极性键构成的分子,结构对称,正负电荷的中心重合,则为非极性分子.
解答:
解:A.C2H4中有C、H元素之间形成极性键,且分子结构对称,正负电荷的中心重合,属于非极性分子;C2H2中有C、H元素之间形成极性键,且分子结构对称,正负电荷的中心重合,属于非极性分子;CO2中有C、O元素之间形成极性键,且分子结构对称,正负电荷的中心重合,属于非极性分子,故A正确;
B.CH4 中含有极性键,为正四面体结构,结构对称,分子中正负电荷重心重叠,为非极性分子;CHCl3有C、H和C、O元素之间形成极性键;但结构不对称,正负电荷的中心不重合,属于极性分子,故B错误;
C.Cl2中只有Cl﹣Cl非极性键,属于非极性分子;H2中只有H﹣H非极性键,属于非极性分子;N2中只有N﹣N非极性键,属于非极性分子,故C错误;
D.NH3中有N、H元素形成的极性键,但结构不对称,属于极性分子;H2O中H、O元素形成的极性键,但结构不对称,属于极性分子;SO2中有S、O元素之间形成极性键,但结构不对称,正负电荷的中心不重合,属于极性分子,故D错误;
故选A.
点评:
本题考查化学键及分子的极性,明确化学键判断的方法及分子极性的判断方法是解答本题的关键,应熟悉常见分子的构型,题目难度不大.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
实验室因需使用0.100mol/L的Na2CO3溶液400mL而配制
相应溶液,请回答下列问题:
①用天平准确称取Na2CO3固体 g,放入小烧杯中,加适量蒸馏水溶解.
②将①所得的溶液转移至 mL容量瓶中.
③用适量的蒸馏水洗涤 2~3次,并把洗涤液小心的注入容量瓶中,轻轻振荡.
④继续向容量瓶中缓缓加入蒸馏水至液面距离刻度线1~2cm处,改用 逐滴滴加蒸馏水至溶液的凹液面正好与刻度线相切.若不慎超出该如何处理? .
⑤把容量瓶塞盖好,反复上下颠倒,充分摇匀.最后若发现液面低于刻度线,还需补充加水吗?(填“需要”或“不需要”) .
⑥以下问题请在“A.偏小”“B.偏大”“C.无影响”中选择最合适的字母填空
(1)容量瓶在使用之前需加少量蒸馏水进行“检漏”操作,这会造成容量瓶潮湿,则所得溶液的浓度会 ;
(2)有些固体溶解会放热,若未经冷却即转移至容量瓶,则所得溶液的浓度会 ;
(3)若未经洗涤或洗涤液在转移时不慎洒在了实验桌上,则所得溶液的浓度会 .
查看答案和解析>>
科目:高中化学 来源: 题型:
右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答
下列问题:

(1)该浓盐酸的物质的量浓度为___________mol/L。
(2)某学生欲用上述浓盐酸和蒸馏水配制250 mL物质的量浓度为
0.7 mol/L稀盐酸。
①该学生用量筒量取________ mL上述浓盐酸进行配制;
②所需的实验仪器有:①胶头滴管、②烧杯、③量筒、④玻璃棒,配制稀盐酸时,还缺少的仪器有 。
③下列操作导致所配制的稀盐酸的物质的量浓度偏低的是 (填字母)。
A、用量筒量取浓盐酸时俯视凹液面
B、未恢复到室温就将溶液注入容量瓶并进行定容
C、容量瓶用蒸馏水洗后未干燥
D、定容时仰视液面
E、未洗涤烧杯和玻璃棒
(3)若在标准状况下,将a L HCl气体溶于1 L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为  mol/L。
mol/L。
a.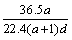 b.
b.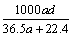 c.
c.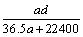 d.
d.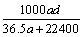
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验事实得出的结论不正确的是 ( )
| 选项 | 实验事实 | 结论 |
| A | H2可在Cl2中燃烧 | 燃烧不一定有氧气参加 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 氧化铝熔点高于铝 |
| C | 将SO2通入含HClO的溶液中,生成H2SO4 | HClO酸性比H2SO4强 |
| D | 向FeCl2溶液中滴入KSCN溶液,在液面出现微红色 | Fe2+在空气中被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将11g铝铁合金的粉末放入100mL过量的KOH溶液
中充分反应,得到标准状况下6.72L H2。试计算:
(1)该合金中铝的质量分数(保留两位有效数字);
(2)该合金中铝和铁的物质的量之比。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的熔点或液化温度由高到低顺序的是( )
|
| A. | 金刚石>晶体硅>碳化硅 | B. | CF4>CCl4>CBr4 |
|
| C. | NH3>N2>H2 | D. | 纯镁>镁铝合金>纯铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的性质与氢键无关的是( )
|
| A. | 冰的密度比液态水的密度小 |
|
| B. | NH3易液化 |
|
| C. | NH3分子比PH3分子稳定 |
|
| D. | 在相同条件下,H2O的沸点比H2S的沸点高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验事实与平衡移动无关的是( )
|
| A. | 氯气难溶于饱和食盐水 |
|
| B. | 用加压的方法促进CO2在水中的溶解 |
|
| C. | FeCl3+3KSCN⇌Fe(SCN)3+KCl,向体系中加入KCl固体 |
|
| D. | 合成氨工业中,及时将氨气液化移出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com