
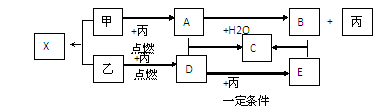
| A.化合反应 | B.氧化还原反应 | C.非氧化还原反应 | D.离子反应 |


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源:不详 题型:单选题
| A.单质都能在O2中燃烧生成过氧化物。 |
| B.从Li到Cs,密度越来越大,熔点越来越低。 |
| C.单质都可以保存在煤油中。 |
| D.单质都是强还原剂,与水反应都生成强碱。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.可能存在核外电子排布式为1s22s22p63s23p64s24p1的原子 |
| B.当电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,而且自旋方向相反 |
| C.1个原子轨道里最多容纳2个电子,且自旋方向相同 |
| D.基态原子的电子获得一定能量变为激发态原子,而激发态原子变为基态原子,则要放出能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.它们都能与水反应生成氢气和碱 |
| B.所形成的阳离子的氧化性随原子序数递增依次减弱 |
| C.它们在空气中燃烧都生成R2O(R指碱金属) |
| D.碱金属中密度最小、熔沸点最高的是锂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
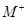 、
、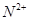 、
、 、
、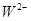 具有相同的电子层结构。(用推断出的元素符号表示)
具有相同的电子层结构。(用推断出的元素符号表示)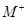 、
、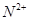 、
、 、
、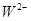 的离子半径由大到小的顺序是? ?。
的离子半径由大到小的顺序是? ?。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转 |
| B.电子从低能级跃迁到高能级的过程中一定要释放能量 |
| C.在同一能级上运动的电子,其运动状态一定完全相同 |
| D.能量低的电子在离核近的区域运动,能量高的电子在离核远的区域运动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.共有7个周期,16个族 |
| B.形成化合物种类最多的元素在第二周期 |
| C.第ⅡA族的右边是第ⅢB族,第ⅢA族的左边是第ⅡB族 |
| D.某主族元素最高价氧化物对应的水化物的化学式为HnROm,其气态氢化物的化学式一定为H2m-nR或RH2m-n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com