
| A、2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ |
| B、H2O2+H2SO4═SO2+O2+2H2O |
| C、I2+SO2+2H2O═H2SO4+2HI |
| D、2Fe3++H2O2═2Fe2++O2↑+2H+ |


科目:高中化学 来源: 题型:
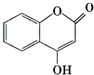 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成: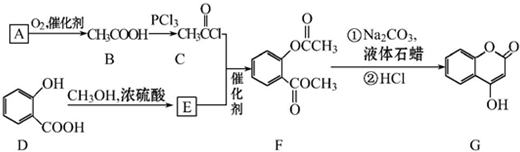
查看答案和解析>>
科目:高中化学 来源: 题型:
| Cl2 |
| ① |
| 480-530℃ |
| ② |
| 聚合 |
| 2200℃~2300℃ |
| HgCl2 |
| 140℃~200℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
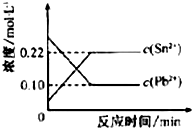 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )| A、往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B、往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C、升高温度,平衡体系中c(Pb2+)增大,说明该反应为吸热反应 |
| D、25℃时,该反应的平衡常数K=2.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从铝土矿中分离出氧化铝的过程中不涉及氧化还原反应 |
| B、纯净的二氧化硅有优良的光学性能,可制成光电池和光导纤维 |
| C、海水中含有大量的钠元素,只需经过物理变化就可以得到钠单质 |
| D、Na+、Mg2+、Al3+得电子能力很弱,故常用电解熔融氧化物的方法来制备其单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该电池工作时,正极反应为:2AgCl+2e-═2C1-+2Ag |
| B、该电池的负极材料可以用金属铝代替 |
| C、有24g Mg被氧化时,可还原得到108gAg |
| D、装备该电池的鱼雷在水中行进时,海水作为电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,16 g O3气体含有氧原子数为NA |
| B、标准况状下,44.8 L四氯化碳含有的分子数为2NA |
| C、0.5 mol H2的质量为1 g,体积为11.2 L |
| D、2.4 g金属镁变为镁离子时失去的电子数为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com