
【题目】固定和利用CO2能有效地利用资源,并减少空气中的温室气体.工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣49kJ/mol.某科学实验在一定温度下,将6molCO2和8molH2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.a,b,c,d括号内数据表示坐标. 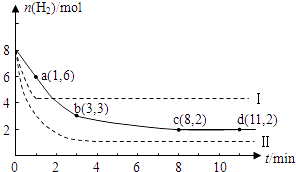
(1)0~a,a~b,b~c,c~d四段中,平均反应速率最大的时间段是 , 该时间段内H2的平均反应速率是 .
(2)a点正反应速率(填大于、等于或小于)逆反应速率.
(3)平衡时CO2的转化率是;反应前、后容器内的压强比是 .
【答案】
(1)0~a;1mol/(L?min)
(2)大于
(3)33.3%;7:5
【解析】解:(1)a点时还没有达到平衡状态,反应物氢气的物质的量继续减小,平衡向正向移动,所以正反应速率大于逆反应速率,分别计算不同时间内的反应速率:0~1min内,v(H2)= ![]() =1mol/(Lmin);8min后达到化学平衡状态,正逆反应速率相等,综合速率为零;所以0~1min内反应速率最大,8~11min反应速率最小, 所以答案是:0~a;1mol/(Lmin);(2)根据图示a点不是平衡状态,反应继续正向进行,所以正反应速率大于逆反应速率,所以答案是:大于;
=1mol/(Lmin);8min后达到化学平衡状态,正逆反应速率相等,综合速率为零;所以0~1min内反应速率最大,8~11min反应速率最小, 所以答案是:0~a;1mol/(Lmin);(2)根据图示a点不是平衡状态,反应继续正向进行,所以正反应速率大于逆反应速率,所以答案是:大于;
·(3)
CO2(g)+ | 3H2(g) | CH3OH(g)+ | H2O(g) | ||
起始物质的量/mol | 6 | 88 | 0 | 0 | |
物质的量变化/mol | 2 | 6 | 2 | 2 | |
平衡物质的量/mol | 4 | 2 | 2 | 2 |
二氧化碳的转化率= ![]() ×100%=33.3%,反应前后容器内的压强比等于气体物质的量之比:P前:P后=(6+8):(4+2+2+2)=14:10=7:5;
×100%=33.3%,反应前后容器内的压强比等于气体物质的量之比:P前:P后=(6+8):(4+2+2+2)=14:10=7:5;
所以答案是:33%;7:5.
【考点精析】通过灵活运用化学平衡状态本质及特征,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)即可以解答此题.


科目:高中化学 来源: 题型:
【题目】下列离子方程式中书写正确的有几项
① FeS固体与稀硝酸混合:FeS + 2H+ = Fe2++H2S
② 用过量氨水吸收烟道气中的SO2:SO2+2NH3·H2O =SO32-+2NH4++H2O
③ 将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO32-+2HClO
④ 已知Ka1(H2CO3)> Ka(HClO)> Ka2(HCO3-),向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32-
⑤ 铁屑溶于足量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
⑥ 氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
⑦ 实验室用NH4Cl和Ca(OH)2制氨气:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
⑧ 向NH4Al(SO4)2溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O
⑨ 实验室制Cl2:4HCl(浓)十MnO2![]() Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
⑩ FeCl3溶液刻蚀铜制电路板:Fe3+ +Cu = Fe2+ + Cu2+
A. 1 项 B. 2 项 C. 3 项 D. 4 项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能获得成功的是( )
A. 溴苯中含有溴单质,可用NaOH溶液洗涤,再经分液而除去
B. 制硝基苯时,在浓硫酸中加入浓硝酸后,立即加苯混合,进行振荡
C. 在酸性高锰酸钾溶液中滴加几滴苯,用力振荡,紫红色褪去
D. 在液体苯中通氢气可制得环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学进行如下实验,以检验化学反应中的能量变化. 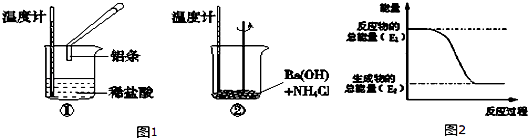
请回答下列问题:
(1)如图1实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是热反应,Ba(OH)28H2O与NH4Cl的反应是热反应.反应过程(填“①”或“②”)的能量变化可用图2表示.
(2)现有如下两个反应: (A)NaOH+HCl=NaCl+H2O (B)2FeCl3+Cu=2FeCl2+CuCl2
以上两个反应能设计成原电池的是 , 负极材料为: , 电解质溶液为: , 正极的电极反应式为:;负极的电极反应式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
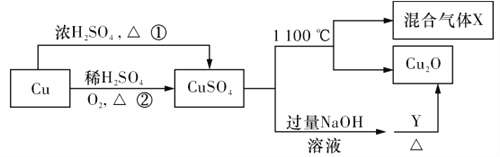
A. 相对于途径①,途径②更好地体现了绿色化学思想
B. Y可以是葡萄糖溶液
C. CuSO4在1100℃分解所得气体X是SO2和SO3的混合气体
D. 将CuSO4溶液蒸发浓缩、冷却结晶可制得胆矾晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成药物的中间体M的合成路线如下:
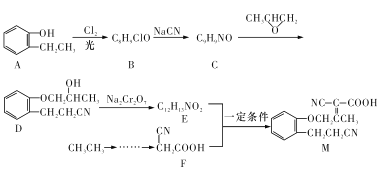
已知:①RX![]() RCN; ②RCH2COOH
RCN; ②RCH2COOH![]()
![]() 。
。
请回答:
(1)D→E的反应类型是_______________。
(2)下列说法不正确的是_____________(填字母)。
A.化合物B的官能团有羟基和氯原子
B.1 mol化合物B最多可消耗3 mol NaOH
C.化合物C至少有12个原子在同一平面
D.化合物D能发生加成反应和消去反应
(3)写出E+F→M的化学反应方程式:_____________________________。
(4)写出符合下列条件的C的所有同分异构体:![]() 、
、 、
、 、________。
、________。
①分子中除苯环外还含有五元环,是苯环的邻位二取代物;
②IR谱显示存在(C=N),且能发生银镜反应。
(5)请结合题给信息,设计以CH3CH2Cl为原料制备F的合成路线(用流程图表示,无机试剂任选)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不能用勒夏特列原理解释的是
A. 新制氯水光照后颜色变浅
B. 2HI(g)![]() H2(g)+I2(g)平衡体系,加压颜色变深
H2(g)+I2(g)平衡体系,加压颜色变深
C. 高压比常压有利于合成氨
D. 钠与氯化钾共融制备钾Na(1)+KCl(l)![]() K(g)+NaCl(l)
K(g)+NaCl(l)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com