
50mL pH=1的稀硫酸和盐酸的混合液与50mLBa(OH)2溶液相混合,充分反应后过滤,得0.446g沉淀,滤液的pH变为13.求:
(1)原混合酸液中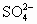 和Cl-的物质的量.
和Cl-的物质的量.
(2)Ba(OH)2溶液的物质的量浓度.
|
【答案】(1)0.002mol,0.001mol;(2)0.015mol/L 【解析】这是一道关于溶液浓度和pH的计算题.将稀硫酸和盐酸的混合液与50mL Ba(OH)2溶液相混合,离子间发生的反应有:Ba2++ n(H2SO4)=n(BaSO4)= 硫酸电离出的n( 而稀硫酸和盐酸的混合液为50mL pH=1,共有n(H+)=0.05L×0.1mol/L=0.005mol,所以盐酸电离出的n(H+)=0.005mol-0.004mol=0.001mol,n(Cl-)=0.001mol. 反应后滤液的pH变为13,呈碱性,说明Ba(OH)2溶液过量,反应后过量的n(OH-)=0.1L×0.1mol/L=0.01mol,反应了的n(OH-)=n(H+)=0.005mol,所以Ba(OH)2中的n(OH-)=0.01mol+0.005mol=0.015mol,可求出 c[Ba(OH)2]= |
|
【方法提炼】审题是解题中至关重要的一环.如此题中由沉淀的质量立即明确了这是硫酸钡,进而求出硫酸、硫酸根等.由滤液的pH变为13发现酸碱并非恰好完全中和,而是Ba(OH)2过量,通过n(OH-)的计算可求出Ba(OH)2溶液的物质的量浓度. |


科目:高中化学 来源: 题型:013
下列溶液混合后,pH值最大的是( )
A.![]() 与0.2mol/L氨水各50ml
与0.2mol/L氨水各50ml
B.![]() 与0.1mol/NaOH溶液各50ml
与0.1mol/NaOH溶液各50ml
C.pH=1的![]() 与pH=13的NaOH溶液各50ml
与pH=13的NaOH溶液各50ml
D.pH=1的盐酸与pH=13的NaOH溶液各50m1
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
A.![]() 与0.2mol/L氨水各50ml
与0.2mol/L氨水各50ml
B.![]() 与0.1mol/NaOH溶液各50ml
与0.1mol/NaOH溶液各50ml
C.pH=1的![]() 与pH=13的NaOH溶液各50ml
与pH=13的NaOH溶液各50ml
D.pH=1的盐酸与pH=13的NaOH溶液各50m1
查看答案和解析>>
科目:高中化学 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高二化学(上) 题型:022
称取三份锌粉,分盛于甲、乙、丙三支试管中,按下列要求另加物质后,塞上导管塞子,定时测定生成的氢气的体积.甲加入50mL pH=3的盐酸,乙加入50mL pH=3的CH3COOH,丙加入50mL pH=3的CH3COOH及少量胆矾粉末,若反应终了,生成氢气的体积一样多,且没有剩余的Zn,请用“>”,“=”或“<”回答:
(1)开始时反应速率的大小为________.
(2)三试管中参加反应的锌的质量为________.
(3)反应终了,所需时间为________.
(4)在反应过程中,乙、丙速率不同的理由(简要说明)是________.
查看答案和解析>>
科目:高中化学 来源:2015届四川省高二上学期第三次月考化学试卷(解析版) 题型:选择题
pH=1的两种一元酸HX与HY溶液,分别取50mL加入足量镁粉,充分反应后,收集到H2体积分别为V1和V2 。若V1>V2,则下列说法正确的是
A.两酸的浓度大小c(HX)<c(HY)
B.等浓度时HX溶液的酸性比HY溶液的酸性弱
C.HX可能是强酸
D.将两种一元酸均稀释100倍,稀释后两溶液的pH均为3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com