
醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是
A.醋酸溶液中:c(H+)>c(CH3COO-)>c(OH-)
B.NaHCO3溶液中:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-)
C.等体积、等物质的量浓度的醋酸与氢氧化钠溶液混合:c(Na+)=c(CH3COO-)
D.中和等体积、等物质的量浓度的CH3COOH溶液和HCl溶液所消耗的NaOH物质的量相等
AD
【解析】
试题分析:醋酸溶液中醋酸能部分电离出醋酸根离子和氢离子,水也能微弱地电离出氢离子和氢氧根离子,但前者的电离程度大于后者,所以该溶液中c(H+)>c(CH3COO-)>c(OH-),故A正确;碳酸氢钠能完全电离出钠离子和碳酸氢根离子,水也能微弱地电离出氢离子和氢氧根离子,但前者的电离程度大于后者,碳酸氢根离子既能电离又能水解,水电离出的氢离子有一部分没有被消耗,另一部分氢离子与水解的碳酸氢根离子结合生成H2CO3,水电离出的氢氧根离子也有一部分没有被消耗,另一部分与碳酸氢根离子中和生成碳酸根离子,和水,即H++ HCO3-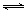 H2CO3、OH-+ HCO3-
H2CO3、OH-+ HCO3-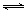 CO32-+H2O,则水电离出c(H+)=溶液中的c(H+)+c(H2CO3),水电离出的c(OH-)=溶液中的c(OH-)+c(CO32-),由于H2O
CO32-+H2O,则水电离出c(H+)=溶液中的c(H+)+c(H2CO3),水电离出的c(OH-)=溶液中的c(OH-)+c(CO32-),由于H2O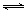 H++OH-中各物质的系数之比等于物质的量浓度之比,则由水电离出的c(OH-)= 水电离出的c(H+),即溶液中的c(H+)+c(H2CO3)= 溶液中的c(OH-)+c(CO32-),故B错误;由于n=c•V,则混合前氢氧化钠的物质的量等于醋酸的物质的量,则二者恰好完全中和,得到溶液是醋酸钠溶液。醋酸钠是强碱弱酸盐,能水解,导致混合溶液显碱性,则溶液中c(OH-)>c(H+),混合溶液中只有醋酸根离子、钠离子、氢离子和氢氧根离子,根据电荷守恒原理,则溶液中c(Na+)+ c(H+)= c(OH-)+ c(CH3COO-),由于c(OH-)>c(H+),则溶液中c(Na+)>c(CH3COO-),故C错误;c1• V1 =c2•V2,则醋酸的物质的量与氯化氢相等,由于CH3COO+NaOH=CH3COOH+H2O、HCl+NaOH=NaCl+H2O,其中各物质的系数之比等于物质的量之比,则两反应完全中和时消耗NaOH的物质的量相等,故D正确。
H++OH-中各物质的系数之比等于物质的量浓度之比,则由水电离出的c(OH-)= 水电离出的c(H+),即溶液中的c(H+)+c(H2CO3)= 溶液中的c(OH-)+c(CO32-),故B错误;由于n=c•V,则混合前氢氧化钠的物质的量等于醋酸的物质的量,则二者恰好完全中和,得到溶液是醋酸钠溶液。醋酸钠是强碱弱酸盐,能水解,导致混合溶液显碱性,则溶液中c(OH-)>c(H+),混合溶液中只有醋酸根离子、钠离子、氢离子和氢氧根离子,根据电荷守恒原理,则溶液中c(Na+)+ c(H+)= c(OH-)+ c(CH3COO-),由于c(OH-)>c(H+),则溶液中c(Na+)>c(CH3COO-),故C错误;c1• V1 =c2•V2,则醋酸的物质的量与氯化氢相等,由于CH3COO+NaOH=CH3COOH+H2O、HCl+NaOH=NaCl+H2O,其中各物质的系数之比等于物质的量之比,则两反应完全中和时消耗NaOH的物质的量相等,故D正确。
考点:考查溶液中粒子浓度大小关系,涉及电离程度的判断、质子守恒原理、酸碱中和反应、盐类水解、电荷守恒定律、强电解质、弱电解质等。


科目:高中化学 来源:2015届江苏省江宁分校高二上学期选修期末化学试卷(解析版) 题型:选择题
盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是
A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH-
B.NaHCO3溶液中:c (H+)+c (Na+)= c (HCO3-)+2c(CO32-)+c(OH-)
C.中和体积与物质的量浓度都相同的HCl溶液和CH3COOH溶液消耗NaOH物质的量相同
D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗NaOH物质的量相同
查看答案和解析>>
科目:高中化学 来源:2010--2011学年四川省高二上学期期中考试化学试卷 题型:选择题
盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是( )
A.0.2 mol / L醋酸与0.1 mol / L醋酸中c(H+)之比为2∶1
B.NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)
C.CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.中和体积与pH都相同的HCl溶液和CH3COOH溶液,所消耗的NaOH物质的量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com