
分析 (1)水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;
在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物既不是电解质,也不是非电解质;物质导电有两种原因:一是金属类有自由移动的电子能够导电,二是能够产生自由离子的溶液能够导电;
(2)二氧化硫是导致酸雨的气体;二氧化硅可以制光导纤维;三氧化二铝具有两性;三氧化二铁是红棕色的固体;
(3)五颜六色的焰火利用了部分金属元素的焰色反应;城市射灯在夜空形成五颜六色的光柱,是胶体的丁达尔效应;
(4)氢氧化铝具有弱碱性,与盐酸反应生成氯化铝与水,可以治疗胃酸过多;
碳酸氢钠具有弱碱性,与盐酸反应生成氯化钠、二氧化碳与水,可以治疗胃酸过多.
解答 解:(1)①氯气是单质,既不是电解质,也不是非电解质,氯气不能导电;
②铜是金属单质,既不是电解质,也不是非电解质,铜能导电;
③碳酸钙是盐,在水溶液中虽难溶,但熔化状态下都能完全电离出自由移动的离子而导电,是电解质;碳酸钙固体没有自由移动的离子,不能导电;
④蔗糖是以分子的形式分散在水中形成的溶液不能导电,不属于电解质,属非电解质;蔗糖固体以分子的形式存在不导电;
⑤HCl气体不能导电,溶于水能导电,属于电解质;
⑥SO2不能导电,溶于水能导电是因为生成了亚硫酸,亚硫酸导电,SO2是非电解质;
⑦氨水是氨气溶于水形成的混合物,既不是电解质,也不是非电解质,但是溶液中存在自由移动的离子,能导电;
故答案为:②⑦;③⑤;
(2)二氧化硫能溶于形成亚硫酸,又可以被氧化为硫酸,是导致酸雨的主要气体物质;二氧化硅可以制光导纤维;氢氧化铝既能和强酸反应又能和强碱反应生成盐和水;三氧化二铁是一种红棕色的固体物质;
故答案为:③,②,⑧,⑤;
(3)节日焰火利用的是焰色反应,城市射灯在夜空形成五颜六色的光柱,属于丁达尔效应;
故答案为:焰色;丁达尔;
(4)氢氧化铝具有弱碱性,与盐酸反应生成氯化铝与水,反应方程式为:Al(OH)3+3HCl═AlCl3+3H2O,故可以治疗胃酸过多;碳酸氢钠具有弱碱性,与盐酸反应生成氯化钠、二氧化碳与水,反应离子方程式为:HCO3-+H+=H2O+CO2↑,故可以治疗胃酸过多;
故答案为:Al(OH)3+3H+=Al3++3H2O;HCO3-+H+=H2O+CO2↑.
点评 本题考查了电解质的判断、焰色反应、铝元素及其化合物的性质,难度不大,注意抗酸药不能有腐蚀性.


科目:高中化学 来源: 题型:选择题
| A. | 实验内容未严格规定试剂用量的,可任意取用 | |
| B. | 实验室里的药品除蔗糖、葡萄糖外一律不得品尝 | |
| C. | 一般先用蒸馏水把PH试纸润湿,然后再伸入溶液中检验溶液的酸碱性 | |
| D. | 取用固体试剂时不可用手拿,应用镊子或药匙取用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
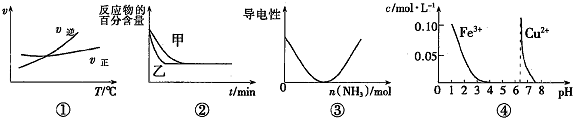
| A. | 据图①可判断可逆反应A2(g)+3B2(g)?2AB3(g)的△H>0 | |
| B. | 图②表示压强对可逆反应2A(g)+B(g)?3C(g)+D(s)的影响,乙的压强大 | |
| C. | 图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 | |
| D. | 据图④,若除去0.1 mol•L-1CuSO4溶液中混有的Fe3+,可向溶液中加入适量NaOH至pH约为7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水形成氯水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 将FeO溶解于足量稀HNO3中:FeO+2H+═Fe2++H2O | |
| C. | 硫酸铝溶液中滴加过量浓氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | SO2用过量NaOH溶液吸收:SO2+2OH-═SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温时,非金属元素的单质都是气体 | |
| B. | 同一周期中,碱金属的第一电离能最小 | |
| C. | VIA 族元素的原子,其半径越大,越容易得到电子 | |
| D. | 同周期元素中,VIIA 族元素的原子半径最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
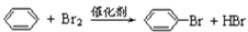 .
.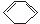 )脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯稳定(填稳定或不稳定).
)脱去2mol氢原子变成苯却放热,可推断苯比1,3-环己二烯稳定(填稳定或不稳定).
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S溶液的水解:S2-+2H2O?H2S+2OH- | |
| B. | NaHCO3溶液的电离:HCO3-+H2O?H2 CO3+OH- | |
| C. | NH4Cl溶液的水解:NH4++H2O?NH3•H2O+H+ | |
| D. | 泡沫灭火器灭火原理:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com