
“摩尔盐”[ (NH4)2Fe(SO4)2·6H2O ] 是分析化学中的重要试剂。查阅文献得知:“摩尔盐”隔绝空气加热至500℃时可完全分解,但产物复杂。某学习小组欲探究其分解产物。
Ⅰ.【提出猜想】摩尔盐受热分解,小组同学认为分解产物可能有以下几种情况:
a.Fe2O3、SO3、NH3、H2O b.FeO、NH3、SO3、H2O
c.FeO、SO2、NH3、H2O d.Fe2O3、NH3、SO2、SO3、H2O
经认真分析,通过推理即可确定,猜想 不成立(填序号)。
Ⅱ.【实验探究】为检验分解产物,甲同学设计了如下实验装置。
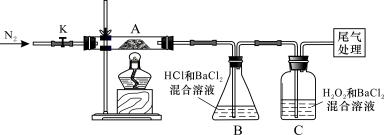
请回答下列问题:
(1)B装置的容器名称是 。
(2)取一定量“摩尔盐”置于加热管A中,加热至分解完后打开K,再通入N2,目的是 。
(3)观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀。C中发生反应的离子方程式为_________________________。
(4)待A中剩余固体冷却至室温后,取少量置于试管中,加入稀硫酸溶解,再滴几滴KSCN溶液,可以观察到的现象是 。
(5)乙同学设计实验验证A中残留物不含FeO,操作方法及实验现象是:取少量A中残留物放入试管中, 。
Ⅲ.【实验反思】
乙同学认为:装置B中产生白色沉淀不能证明分解产物中一定含SO3,原因是 。
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源:2014-2015学年湖南省益阳市高三四月调研考试理综化学试卷(解析版) 题型:选择题
心酮胺是治疗冠心病的药物,其结构简式如下图,下列描述中正确的是
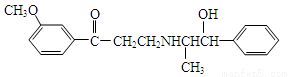
A.该分子中含有酚羟基
B.该物质可以和浓氢溴酸发生取代反应
C.该物质可以和银氨溶液发生银镜反应
D.该分子苯环上的一氯取代物有6种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河西区高三下学期总复习质量调查(二)化学试卷(解析版) 题型:选择题
臭氧在烟气脱硝中的反应为2NO2(g) + O3(g) N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是
N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,相关图象如下列选项,其中对应分析结论正确的是
A | B | C | D |
|
|
|
|
平衡后升温, NO2含量降低 | 0~2 S内, v(O3)=0.2 mol·L-1·s-1 | v正 :b点> a点 b点:v逆 > v正 | 恒温, t1时再充入O3 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三下学期第二次月考化学试卷(解析版) 题型:简答题
液晶高分子材料应用广泛。新型液晶基元——化合物Ⅳ的合成线路如下:
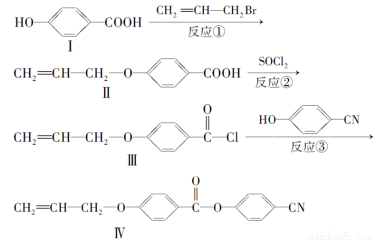
(1)化合物Ⅰ的分子式为________,1 mol化合物Ⅰ最多可与________mol NaOH反应。
(2)CH2=CH—CH2Br与NaOH水溶液反应的化学方程式为(注明条件)______________。
(3)化合物Ⅰ的同分异构体中,苯环上一溴代物只有2种且能发生银镜反应的化合物有多种,写出其中一种同分异体的结构简式____________________。
(4)下列关于化合物Ⅱ的说法正确的是_______(填字母)。
A.属于烯烃 B.能与FeCl3溶液反应显紫色
C.一定条件下能发生加聚反应 D.能使溴的四氯化碳溶液褪色
(5)反应③的反应类型是________。在一定条件下,化合物 也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ。Ⅴ的结构简式是__________。
也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ。Ⅴ的结构简式是__________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三下学期第二次月考化学试卷(解析版) 题型:选择题
下列反应的离子方程式表示不正确的是
A.漂白粉溶液在空气中长时间放置:ClO-+CO2+H2O = HClO+HCO
B.FeBr2溶液中通入少量Cl2:2Fe2++Cl2 =2Fe3++2Cl-
C.AgNO3溶液中加入过量稀氨水:Ag++2NH3·H2O = [Ag(NH3)2]++2H2O
D.SO2使氯水褪色:SO2+Cl2+2H2O =SO42-+2Cl-+4H+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省绵阳市高三第三次诊断性考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法不正确的是
A.46 g C2H6O中含有的C-H键数一定为5NA
B.常温常压下,17 g甲基(-14CH3)所含电子总数为9NA
C.标准状况下,11.2 L CO2和乙炔的混合气体所含π键数目为NA
D.CO2气体与足量的Na2O2反应,固体增重28 g时转移了NA个电子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省达州市第二次诊断性测试化学试卷(解析版) 题型:简答题
(14分)已知ABCDEF六种元素的原子序数依次增加,ABCD位于前三周期A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子总数是未成对电子总数的3倍ABD三种元素组成的一种化合物M可用于配制化妆品,是皂化反应的产物之一;AB两种元素组成的原子个数比为1:1的化合物N是常见的有机溶剂E有“生物金属”之称,E 离子和氩原子的核外电子排布相同,元素F的三价阳离子3d轨道处于半充满状态请回答下列问题(答题时,ABCDEF用所对应的元素符号表示)
离子和氩原子的核外电子排布相同,元素F的三价阳离子3d轨道处于半充满状态请回答下列问题(答题时,ABCDEF用所对应的元素符号表示)
(1)E的基态原子的外围电子排布式为
(2)上述非金属元素中电离能最大的元素是
(3)下列叙述正确的是 (填字母)
a.M与水分子间能形成氢键,N是非极性分子
b.M和BD2分子中的中心原子均采用sp2杂化
c.N分子中含有6个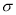 键和1个
键和1个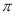 键
键
d.BD2晶体的熔点沸点都比二氧化硅晶体的低
(4)与BCD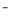 互为等电子体的微粒的化学式为 (任写一种)
互为等电子体的微粒的化学式为 (任写一种)
(5)在浓的ECl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6组成为ECl3·6H20的绿色晶体,该晶体属于配合物,有两种配体,其物质的量之比为1:5,则该配离子的化学式为
(6)电镀厂排放的废水中常含有剧毒的BC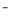 离子,可在催化剂的催化下,先用NaClO将BC
离子,可在催化剂的催化下,先用NaClO将BC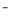 氧化成BCD
氧化成BCD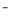 ,再在酸性条件下BCD
,再在酸性条件下BCD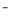 继续被NaClO氧化成C2和BD2则后一步反应的离子方程式是
继续被NaClO氧化成C2和BD2则后一步反应的离子方程式是
(7)F的低价硫酸盐的溶液在空气中易变质,检验其在空气中是否已完全变质的实验操作是 (要求写出操作现象结论)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:选择题
向等物质的量浓度的NaOH和Ca(OH)2的混合液中通入一定量CO2。下列离子方程式与事实不相符的是
A.OH-+CO2 → HCO3-
B.2OH-+CO2 → CO32-+H2O
C.Ca2++2OH-+CO2 → CaCO3↓+H2O
D.Ca2++4OH-+2CO2 → CaCO3↓+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:选择题
科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验。羟基硝酸铵的结构如图所示,下列说法不正确的是
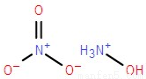
A.羟基硝酸铵中阳离子的各原子共平面
B.羟基硝酸铵是离子化合物
C.羟基硝酸铵中含有离子键和共价键
D.9.6g羟基硝酸铵中含有0.2mol离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com