
| A. | NaHCO3═Na++H++CO32- | B. | NaHSO4═Na++HSO4- | ||
| C. | Al2 (SO4)3═Al 3++SO42- | D. | Na2SO4═2Na++SO42 |
分析 A.碳酸氢根离子是弱酸的酸根离子是一个整体不能拆;
B.硫酸氢钠为强电解质,完全电离生成钠离子、氢离子、硫酸根离子;
C.硫酸铝属于盐,为强电解质,完全电离出铝离子和硫酸根离子,方程式左右电荷不守恒;
D.Na2SO4是强电解质,完全电离生成硫酸根离子、钠离子.
解答 解:A.碳酸氢钠电离时生成钠离子和碳酸氢根离子,碳酸氢根离子是弱酸的酸根离子是一个整体不能拆,电离方程式为NaHCO3═Na++HCO3-,故A错误;
B.硫酸氢钠为强电解质,完全电离,电离方程式:NaHSO4═Na++H++SO42-,故B错误;
C.硫酸铝强电解质,电离时电离出自由移动的铝离子和硫酸根离子,电离方程式为Al2(SO4)3=2Al3++3SO42-,故C错误;
D.Na2SO4是强电解质,完全电离生成硫酸根离子、钠离子,电离方程式为Na2SO4═2Na++SO42-,故D正确;
故选D.
点评 本题考查电离方程式的书写,明确书写方法及弱电解质的电离书写是解答的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
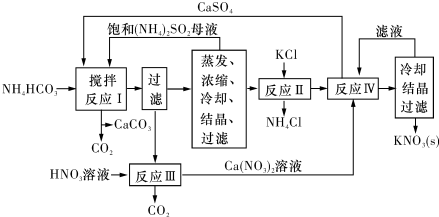
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
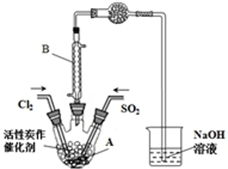 某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示.
某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如表所示. | SO2Cl2 | Cl2 | SO2 | |
| 熔点/℃ | -54.1 | -101 | -72.4 |
| 沸点/℃ | 69.1 | -34.6 | -10 |
| 性质 | 遇水发生剧烈水解 | / | / |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 14C可用于文物年代的鉴定,14C与12C互为同素异形体 | |
| C. | 凡含有添加剂的食物对人体健康均有害,不宜食用 | |
| D. | “开发利用新能源”、“汽车尾气催化净化”都能提高空气质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
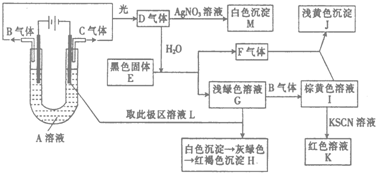
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的还原剂是NH4+ | |
| B. | 消耗1mol氧化剂,转移2mol电子 | |
| C. | 氧化剂与还原剂的物质的量之比是2:3 | |
| D. | 反应后溶液酸性明显增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入KSCN溶液不一定变红色 | B. | 溶液中一定含Fe2+ | ||
| C. | 溶液中一定含Cu2+ | D. | 剩余固体中一定含Cu和Fe |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com