
【题目】乙烯可通过石油裂解获得.下列有关乙烯性质的说法错误的是( )
A.在常温常压下为液体
B.能使酸性KMnO4溶液褪色
C.可自身加成形成聚乙烯
D.能使溴的CCl4溶液褪色
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】氰化钠(NaCN)是一种重要的化工原料、有剧毒,一旦泄露可以通过喷洒双氧水或硫代硫酸钠溶液来处理。
已知:氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3==NaSCN+Na2SO3回答下列问题:
(1)氰化物中碳的化合价为___________;用硫代硫酸钠处理1mol NaCN时,反应中转移电子的物质的量为 。
(2) NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是 。
(3)某化学兴趣小组在实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】制备Na2S2O3,其实验室装置如下:
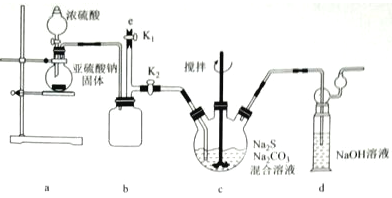
b装置的作用是___________;c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有_____________。
实验结束后,在e处最好连接盛____________(填化学式)的注射器,再关闭K2打开K1,以防拆除装置过程中的有害气体污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先于Ag+反应。
实验如下:取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定时1.000×10-4mol/L的标准AgNO3溶液应用_________(填仪器名称)盛装;滴定终点时的现象是___________。
处理后的废水是否达到排放标准:__________(填“是”或“否”),其依据是__________(用实验数据说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组查阅资料得知:苯和液溴在有溴化铁(FeBr3)存在的条件下可发生反应生成溴苯和溴化氢,此反应为放热反应。他们设计了下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A中。如图是制取溴苯的装置。试回答:
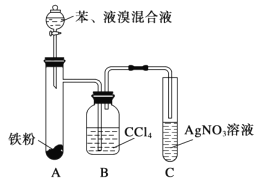
(1)装置A中发生反应的化学方程式是______________________。
(2)装置C中看到的现象是______________,证明________________。
(3)装置B是吸收瓶,内盛CCl4液体。如果没有B装置而将A、C直接相连,你认为是否妥当?__________(填“是”或“否”),理由是_____________________。
(4)实验完毕后将A试管中的液体倒在装有冷水的烧杯中,烧杯_________(填“上”或“下”)层为溴苯,这说明溴苯___________且_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯可通过石油裂解获得。下列有关乙烯的说法错误的是
A. 可以用作为水果的催熟剂
B. 不能使溴的CCl4溶液褪色
C. 能使酸性KMnO4溶液褪色
D. 在一定条件下,可自身加成形成聚乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下CO2和H2可发生反应:CO2(g)+ H2(g)![]() CO (g)+H2O(g) △H
CO (g)+H2O(g) △H
已知:①CO和H2的燃烧热分别为-283.0 kJmol-1 和-285.8kJmol-1
②H2O(l)= H2O(g) △H=+44.0KJ·mol-1
(1)写出表示H2燃烧热的热化学方程式____________________。
CO2(g)+ H2(g)![]() CO(g)+ H2O(g) △H1=___________KJ·mol-1
CO(g)+ H2O(g) △H1=___________KJ·mol-1
(2)有利于提高CO2平衡转化率的措施有__________。
A.加压 B.升温
C.增大CO2浓度 D.投料比不变,增加反应物的浓度
(3)若CO2和H2初始投料比为1:1,反应达平衡时CO在平衡混和气中的体积分数为25%,则CO2的转化率为_________,该反应的平衡常数为_________,若CO2和H2初始投料比改为1:2,则CO2的平衡转化率为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应速率受很多因素影响.下列措施主要是从降低反应速率的角度考虑的是( )
A.将食物置于冰箱中冷藏保存
B.将FeCl3加入H2O2溶液中制备O2
C.将洗衣粉溶于温水后洗涤衣服
D.将CaCO3固体研磨后再与稀HCl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇燃料电池中采用磺酸类质子溶剂,在200 ℃左右时供电,电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图。下列说法中,错误的是
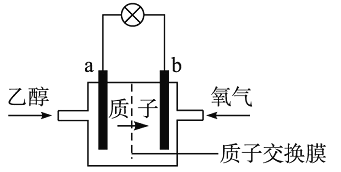
A.电池工作时,质子向电池的正极迁移
B.电池工作时,电流由b极沿导线流向a极
C.a极上发生的电极反应是C2H5OH+3H2O-8e-=2CO2+12H+
D.b极上发生的电极反应是4H++O2+4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】参考下列图表和有关要求回答问题。
(1)图Ⅰ是1 mol NO2(g)和1 molCO(g)反应生成CO2和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________,ΔH的变化是________(填“增大”“减小”或“不变”)。请写出NO2和CO反应的热化学方程式____________________;
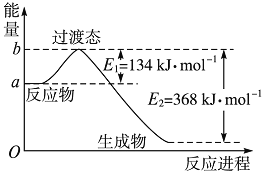
图Ⅰ
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
则甲醇完全燃烧的热化学方程式为________________________;
(3)下表是部分化学键的键能数据:
化学键 | P—P | P—O | O=O | P=O |
键能/(kJ·mol-1) | a | b | c | x |
已知白磷的标准燃烧热ΔH为-d kJ·mol-1,白磷及其完全燃烧的产物结构如图Ⅱ所示,则上表中x=__________kJ·mol-1(用含有a、b、c、d的代数式表示)。
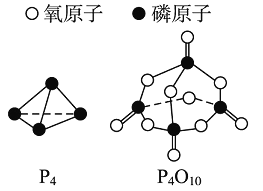
图Ⅱ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com