
HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+.AgNO2是一种难溶于水、易溶于酸的化合物.试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是 (填序号).
A.亚硝酸盐被还原 B.维生素C是还原 剂
剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是 (填序号).
A.测定这两种溶液的pH  B.分别在两种溶液中滴加甲基橙
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI﹣淀粉溶液来区别 D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,请写出反应的离子方程式: .
(4)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是 (填序号).
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2:1,试配平下列方程式:
FeSO4+ K2O2→ K2FeO4+ K2O+ K2SO4+ O2↑
当转移了1.5NA个电子时,在标况下可收集到 升氧气.
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年河北正定中学高一上第一次月考化学试卷(解析版) 题型:选择题
在1 L水溶液中,含有0.1mol氯化钠和0.1mol氯化镁,该溶液中Cl-的物质的量浓度为
A.0.1mol/L
B.0.2mol/L
C.0.3mol/L
D.0.4mol/L
查看答案和解析>>
科目:高中化学 来源:贵州省铜仁市2016-2017学年高一上期中化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.直径介于1nm~100nm之间的微粒称为胶体
B.电泳现象可以证明胶体粒子带电
C.丁达尔效应是溶液与胶体的本质区别
D.胶体粒子很小,可以透过滤纸和半透膜
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三10月月考化学试卷(解析版) 题型:选择题
关于下列各装置的叙述正确的是( )
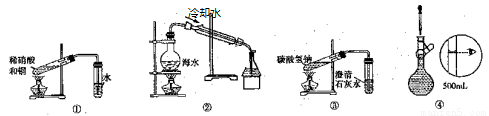
A.装置①可用于实验室制备NO气体
B.装置②可用于模拟海水蒸馏
C.装置③可用于探究碳酸氢钠的热稳定性
D.装置④为配制溶液过程中的定容操作
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三10月月考化学试卷(解析版) 题型:选择题
若NA表示阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,6.72LNO2与水充分反应转移电子数为0.1NA
B.18gD2O中含有的质子数目为10NA
C.常温常压下,1mol氦气中含有的核外电子数为2NA
D.a g某气体含分子 数为b,c g该气体在标况下的体积为22.4ab/(
数为b,c g该气体在标况下的体积为22.4ab/(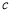 NA)L
NA)L
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上10月模块测试化学试卷(解析版) 题型:选择题
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
⑴4FeO·Cr2O3+8Na2CO3+7O2  8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
⑵2Na2CrO4+H2SO4 Na2SO4+Na2Cr2O7+H2O下列说法中正确的是( )
Na2SO4+Na2Cr2O7+H2O下列说法中正确的是( )
A.反应⑴和⑵均为氧化还原反应
B.反应⑴的氧化剂是O2,还原剂是FeO·Cr2O3
C.高温下,O2的氧化性大于Fe2O3小于Na2CrO4
D.生成1mol的Na2Cr2O7时共转移5mol电子
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上10月模块测试化学试卷(解析版) 题型:选择题
配制一定物质的量浓度的NaOH溶液时,造成实验结果偏低的原因可能是 ( )
A. 容量瓶中原有少量蒸馏水
B. 称量药品时间过长
C. 定容时俯视液面
D. 洗涤烧杯和玻棒的溶液转入容量瓶中;
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上月考二化学卷(解析版) 题型:选择题
现有一块金属钠露置于空气中一段时间,为检验该固体是否部分变质为碳酸钠,先将固体样品溶解于水得到溶液,并采取下列措施,可以实现实验目的是( )
A.测所得溶液的pH
B.取溶液滴入酚酞观察是否变红
C.取 溶液加入盐酸观察是否有气泡
溶液加入盐酸观察是否有气泡
D.取溶液加入CuSO4观察是否有沉淀
查看答案和解析>>
科目:高中化学 来源:2017届江西省赣州市十四校高三上期中联考化学试卷(解析版) 题型:选择题
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为(设反应中HNO3被还原成NO)( )
A. 0.448 L B.0.896 L C.0.672 L D. 0.224L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com