
| A�� | ϡ������0.1 mol/L NaOH��Һ��Ӧ��H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ/mol | |
| B�� | �ܱ������У�9.6 g�����11.2 g���ۻ�ϼ�������������17.6 gʱ���ų�19.12 kJ��������Fe��s��+S��s���TFeS��s����H=-95.6 kJ/mol | |
| C�� | ������ȼ����Ϊ285.8 kJ/mol����ˮ�����Ȼ�ѧ����ʽ��2H2O��l���T2H2��g��+O2��g����H=+285.8 kJ/mol | |
| D�� | ��֪2C��s��+O2��g���T2CO��g����H=-221 kJ/mol�����֪C��ȼ����Ϊ11.5KJ/mol |
���� A��ϡ��ǿ����ǿ������1molH2O�ų�������Ϊ�к��ȣ�ע��������ʵĵ������ȣ�
B������������17.6 g��0.2molʱ���ų�19.12 kJ������ע�����ʵ�״̬����д���Ȼ�ѧ����ʽ��
C��ȼ������ָ��1 mol��ȼ����ȫȼ�������ȶ��Ļ�����ʱ���ų����������ʴ��Ȼ�ѧ����ʽ�ķ�Ӧ����ֵ����
D��ȼ���ȱ�����1mol��ȼ����ȫȼ�������ȶ���������ʱ�ų���������
��� �⣺A��ϡ��ǿ����ǿ������1molH2O�ų�������Ϊ�к��ȣ�������Ϊ������ʣ��������ȣ��ʷ�Ӧ�ȡ�H��-57.3 kJ•mol-1�����Ҵ���Ϊ���ᣬ���ܲ𣬹�A����
B������������17.6 g��0.2molʱ���ų�19.12 kJ������������������1molʱ���ų� 95.6kJ���������Ȼ�ѧ����ʽΪ��Fe��s��+S��s���TFeS��s����H=-95.6 kJ•mol-1����B��ȷ��
C��ȼ���ȱ�����1mol��ȼ����ȫȼ�������ȶ���������ʱ�ų����������������2molH2��ȼ�յ��Ȼ�ѧ����ʽӦΪ��2H2��g��+O2��g��=2H2O��l����H=-571.50kJ•mol-1����ˮ�����Ȼ�ѧ����ʽΪ��2H2O��l���T2H2��g��+O2��g����H=+571.0 kJ•mol-1����C����
D��ȼ���ȱ�����1mol��ȼ����ȫȼ�������ȶ���������ʱ�ų����������˷�Ӧ��̼�IJ���ȫȼ�գ���D����
��ѡB��
���� ���⿼�����к��Ⱥ�ȼ���ȵ��Ȼ�ѧ����ʽ����д��ע���к��Ⱥ�ȼ���ȵĶ���Ҫ�㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
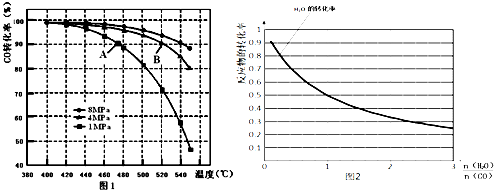
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Zn��s��+CuSO4��aq��=ZnSO4��aq��+Cu��s������H=-216kJ•mol-1����Ӧ��������С�������������� | |
| B�� | ��ͬ�����£����1 mol��ԭ�������е�����ΪE1��1mol����ӵ�����ΪE2����2E1��E2 | |
| C�� | 101kPaʱ��2H2��g��+O2��g��=2H2O��1������H=-571.6kJ•mol-1����������̬ˮ����HС��-571.6kJ•mol-1 | |
| D�� | ����̫���ܵ������Դ���滯ʯȼ�ϣ������ڽ�Լ��Դ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| A | B | C | |
| D | E | F |
 ��ʵ������ȡ����Ļ�ѧ����ʽΪ2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
��ʵ������ȡ����Ļ�ѧ����ʽΪ2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 15 | 20 | 25 | 30 | 35 |
| ƽ����ѹǿ/kPa | 5.7 | 8.3 | 12 | 17.1 | 24 |
| ƽ��������Ũ��/mol•L-1 | 2.4��10-3 | 3.4��10-3 | 4.8��10-3 | 6.8��10-3 | 9.4��10-3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4LH2O���еķ�����ΪNA | |
| B�� | ���³�ѹ�£�32g O2���е���ԭ����Ϊ2NA | |
| C�� | ͨ��״���£�NA��CO2����ռ�е����Ϊ22.4L | |
| D�� | 1L 0.1mol/L NaCl��Һ��������Na+ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KNO3��Һ | B�� | NaCl��Һ | C�� | AgNO3��Һ | D�� | CuCl2��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ӹ������ۣ��ܣ���=�� | B�� | ԭ�Ӹ������ۣ��ܣ��٣��� | ||
| C�� | �� �����ۣ��٣��ܣ��� | D�� | �� �����ۣ��ܣ���=�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com