
对于Na+、Mg2+、Al3+三种离子,下列说法不正确的是( )
A.核外电子层数相同
B.半径大小顺序Na+<Mg2+<Al3+
C.核外电子数相同
D.最外层电子数相同
科目:高中化学 来源:2014年高一化学人教版必修二 2-1化学能与热能练习卷(解析版) 题型:选择题
下列说法正确的是( )
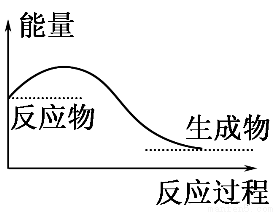
A.任何化学反应都伴随着能量的变化
B.H2O(g)―→H2O(l)的过程放出大量的热,所以该过程是化学变化
C.化学反应中能量的变化都表现为热量的变化
D.如图所示的是吸收能量的过程
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-2-2元素周期律练习卷(解析版) 题型:填空题
元素周期表是学习化学的重要工具,它隐含许多信息和规律。下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为0.089 nm)。
元素代号ABCDE
原子半径/nm0.160.1430.1020.0990.074
主要化合价+2+3+6,-2-1-2
(1)用元素代号标出它们在元素周期表中对应的位置(以下为周期表的一部分)。
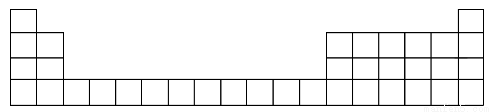
(2)B元素处于周期表中第__________周期、第________族。
(3)B的最高价氧化物对应的水化物与C的最高价氧化物对应的水化物反应的离子方程式为______________。
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是________(填化学式)。
(5)C、E形成的化合物为________(填化学式)。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-2-1原子核外电子排布练习卷(解析版) 题型:选择题
已知某粒子的结构示意图为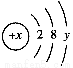 。
。
试回答:
(1)当x-y=10时,该粒子为________(填“原子”“阳离子”或“阴离子”)。
(2)当y=8时,粒子可能为(填粒子符号)______、______、______、______、________。
(3)写出y=3与y=7的元素最高价氧化物对应水化物间发生反应的离子方程式:_________________________________________ _______________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-2-1原子核外电子排布练习卷(解析版) 题型:选择题
下列叙述正确的是( )
A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.两原子,如果核外电子排布相同,则一定属于同种元素
D.只有在原子中,质子数才与核外电子数相等
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-1-3原子结构 核素练习卷(解析版) 题型:填空题
用A.质子数、B.中子数、C.最外层电子数、D.电子层数填写下列空格。
(1)原子种类由________决定。(填写字母序号,下同)
(2)元素种类由________决定。
(3)元素有无同位素由________决定。
(4)1~18号元素的化合价主要由________决定。
(5)元素的化学性质由________决定。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-1-3原子结构 核素练习卷(解析版) 题型:选择题
最近,我国某物理研究所取得重大科技成果,研制出由18O所形成的单质气体。18O是一种稳定的同位素,称为重氧。下列有关说法不正确的是( )
A.1.8 g18O形成的气体的物质的量是0.05 mol
B.0.1 mol重氧水H218O所含的中子数约为6.02×l023个
C.0.2 mol18O2气体的体积约为4.48 L
D.18O2气体的摩尔质量为36 g/mol
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-1-2元素性质练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.F、Cl、Br的最外层电子数都是7,次外层电子数都是8
B.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律
C.卤素按F、Cl、Br、I的顺序其非金属性逐渐减弱的原因是随着核电荷数增加电子层数增大起主要作用
D.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,砹易溶于水,难溶于CCl4
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 模块水平检测2练习卷(解析版) 题型:选择题
目前,医疗上使用放射性核素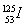 治疗肿瘤,该核素原子核内的中子数与电子数之差是
治疗肿瘤,该核素原子核内的中子数与电子数之差是
A.19 B.53 C.72 D.125
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com