
| A. | 油脂、热的纯碱溶液 | B. | 硫黄、CS2 | ||
| C. | 水垢、食醋 | D. | 石蜡、蒸馏水 |
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、K+、Cl-、SO32- | B. | NH4+、Fe2+、I一、SO42- | ||
| C. | Na+、K+、ClO-、S2- | D. | Na+、S2O32-、AlO2-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
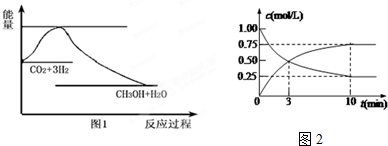
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池能发出蓝色火焰 | B. | H2为正极,O2为负极 | ||
| C. | 正极反应为:O2+2H2O+4e-═4OH- | D. | 正极反应为:2H2+4OH--4e-═4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 | |
| B. | 纯净的H2在Cl2中安静地燃烧,发出苍白色火焰 | |
| C. | 氯气通入品红溶液中,溶液会褪色,是因为氯气具有漂白性 | |
| D. | 氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
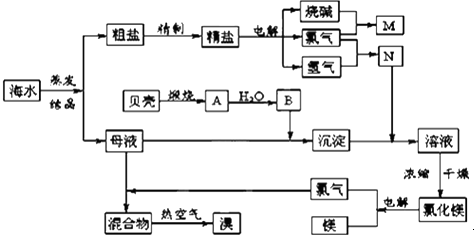
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com