
 CH3OH(g)
CH3OH(g)
| A.升高温度 |
| B.将CH3OH(g)从体系中分离 |
| C.充入He,使体系总压强增大 |
| D.再充入1 mol CO和2 mol H2 |

 BaCO3(s)+SO42-(aq)。
BaCO3(s)+SO42-(aq)。 CH3OH(g) △H=-91kJ/mol (3分,方程式含状态符号正确给1分;反应热2分,其中单位写错扣1分,但结果或符号写错不给分,可逆符号也可以写成等号)
CH3OH(g) △H=-91kJ/mol (3分,方程式含状态符号正确给1分;反应热2分,其中单位写错扣1分,但结果或符号写错不给分,可逆符号也可以写成等号)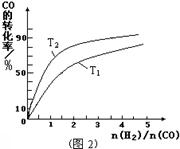
 BaCO3 + SO42-
BaCO3 + SO42-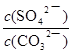 =
=  = 4.0×10-2(2分,单位无写不扣分)
= 4.0×10-2(2分,单位无写不扣分) CH3OH(g) △H=-91kJ/mol;(2)由于正反应是放热反应,其它条件相同时,升高温度平衡向逆反应方向移动,则CO平衡转化率减小,故A错误;甲醇是生成物,从平衡体系移走生成物,减小生成物浓度,平衡向正反应方向移动,反应物平衡转化率增大,故B正确;由于容器容积不变,虽然充入氦气增大压强,但是平衡体系各组分的物质的量、物质的量浓度均不变,所以平衡不能移动,反应物平衡转化率保持不变,故C错误;再充入1molCO和2molH2,就是增大压强,由于正反应是气体体积减小的反应,增大压强平衡向正反应方向移动,反应物的平衡转化率增大,故D正确;(3)读图,横坐标表示氢气和一氧化碳的起始组成比,纵坐标表示CO的平衡转化率;当氢气和一氧化碳的起始组成比为0时,CO的平衡转化率为0;当氢气和一氧化碳的起始组成比相同且不为零时,由于正反应是放热反应,降低温度平衡向正反应方向移动,CO的平衡转化率增大;当氢气和一氧化碳的起始组成比增大时,增大氢气的浓度,平衡向正反应方向移动,CO的平衡转化率增大;根据上述要点作图,可以画出温度为T2时,CO的平衡转化率随氢气和一氧化碳的起始组成比变化的示意图;(4)设硫酸钡溶解的物质的量为xmol,由于BaSO4 + CO32-
CH3OH(g) △H=-91kJ/mol;(2)由于正反应是放热反应,其它条件相同时,升高温度平衡向逆反应方向移动,则CO平衡转化率减小,故A错误;甲醇是生成物,从平衡体系移走生成物,减小生成物浓度,平衡向正反应方向移动,反应物平衡转化率增大,故B正确;由于容器容积不变,虽然充入氦气增大压强,但是平衡体系各组分的物质的量、物质的量浓度均不变,所以平衡不能移动,反应物平衡转化率保持不变,故C错误;再充入1molCO和2molH2,就是增大压强,由于正反应是气体体积减小的反应,增大压强平衡向正反应方向移动,反应物的平衡转化率增大,故D正确;(3)读图,横坐标表示氢气和一氧化碳的起始组成比,纵坐标表示CO的平衡转化率;当氢气和一氧化碳的起始组成比为0时,CO的平衡转化率为0;当氢气和一氧化碳的起始组成比相同且不为零时,由于正反应是放热反应,降低温度平衡向正反应方向移动,CO的平衡转化率增大;当氢气和一氧化碳的起始组成比增大时,增大氢气的浓度,平衡向正反应方向移动,CO的平衡转化率增大;根据上述要点作图,可以画出温度为T2时,CO的平衡转化率随氢气和一氧化碳的起始组成比变化的示意图;(4)设硫酸钡溶解的物质的量为xmol,由于BaSO4 + CO32-  BaCO3 + SO42-中各物质的系数之比等于物质的量之比,则碳酸根离子、硫酸根离子的变化物质的量均为xmol,由于饱和碳酸钠溶液的体积为1L,由于c=n/V,则碳酸根离子、硫酸根离子的变化物质的量浓度均为xmol/L,由此推断该可逆反应中有关组分的(起始、变化、平衡)浓度,则:
BaCO3 + SO42-中各物质的系数之比等于物质的量之比,则碳酸根离子、硫酸根离子的变化物质的量均为xmol,由于饱和碳酸钠溶液的体积为1L,由于c=n/V,则碳酸根离子、硫酸根离子的变化物质的量浓度均为xmol/L,由此推断该可逆反应中有关组分的(起始、变化、平衡)浓度,则: BaCO3 + SO42-
BaCO3 + SO42-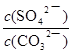 =
=  = 4.0×10-2
= 4.0×10-2

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
| A.增大的CO浓度 | B.增大的H2O(g)浓度 | C.使用催化剂 | D.降低温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (Ka) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
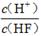 D.
D.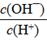
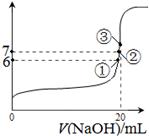
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题
 X(g);△H=-dJ·mol-1(d>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
X(g);△H=-dJ·mol-1(d>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 molA2、1 molBC | 1 molX | 4 molA2、2 molBC |
| 平衡时n(X) | 0.5mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 | α1 | α2 | α3 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
 2CO(g)+2H2(g) 的△H= 。
2CO(g)+2H2(g) 的△H= 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 2NH3(g) △H<0。某实验将3.0 mol N2(g)和4. 0 mol H2(g)充入容积为10L的密闭容器中,在温度T1下反应。测得H2的物质的量随反应时间的变化如下图所示。
2NH3(g) △H<0。某实验将3.0 mol N2(g)和4. 0 mol H2(g)充入容积为10L的密闭容器中,在温度T1下反应。测得H2的物质的量随反应时间的变化如下图所示。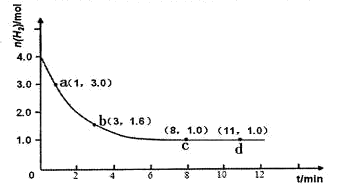

 CH3COO[Cu(NH3)3]?CO △H<0。写出提高CO吸收率的其中一项措施: 。
CH3COO[Cu(NH3)3]?CO △H<0。写出提高CO吸收率的其中一项措施: 。查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 Fe3O4(s)+4H2(g) △H=akJ/mol (I)
Fe3O4(s)+4H2(g) △H=akJ/mol (I) 6FeO(s)+O2(g) △H=bkJ/mol (II)
6FeO(s)+O2(g) △H=bkJ/mol (II)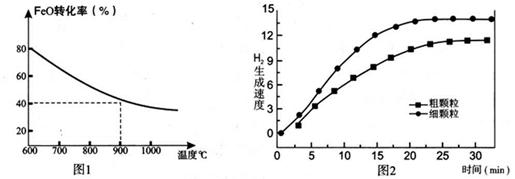
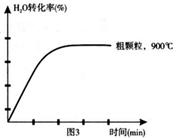
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若A2和B2的总能量之和大于生成的2AB的总能量,则反应放热 |
| B.若A2和B2的总能量之和小于生成的2AB的总能量,则反应放热 |
| C.若该反应为放热反应,则Q1+Q2 < Q3 |
| D.若该反应为吸热反应,则Q1+Q2 < Q3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
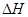 的绝对值均正确)
的绝对值均正确)| A.C2H5OH(l)+3O2(g)==2CO2(g)+3H2O(g);△H=—1367.0 kJ/mol(燃烧热) |
| B.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中和热) |
| C.S(s)+O2(g)===SO2(g);△H=—269.8kJ/mol(反应热) |
| D.2NO2==O2+2NO;△H=+116.2kJ/mol(反应热) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com