
相等物质的量的H2O和H2O2相比较,下列有关叙述中正确的是
①它们所含的分子数目之比为1∶1
②它们所含的原子总数目之比为3∶4
③它们所含的O原子数目之比为1∶2
④它们所含的H原子数目之比为1∶1
⑤它们所含的质子数目之比为5∶9
A.①②③ B.③④⑤ C.①②④ D.①②③④⑤
科目:高中化学 来源:2017届西藏拉萨中学高三上期末理综化学卷(解析版) 题型:推断题
X、Y、Z、Q、W、R六种短周期元素原子序数依次增大。化合物甲由X、Z、Q三种元素组成,常温下0.1mol/L甲溶液的pH=13。工业上常用电解饱和QR溶液生成甲;化合物乙由X、R两种元素组成。请回答下列问题:
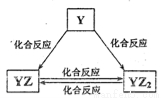
(1)Q的离子结构示意图为____________。
(2)Y元素的单质能发生如图所示的转化,请写出图中反应YZ2→YZ的化学方程式:___________(注明反应条件)。在甲溶液中通入足量YZ2气体,所得溶液呈碱性,写出该溶液中的阴离子浓度由大到小的顺序:______________。
(3)W的单质既能与甲溶液反应,又能与乙溶液反应。
①常温下,将W的单质和甲溶液混合,发生反应的离子方程式为____________;
② Q、W金属性的强弱为Q>W,下列表述中正确的且能证明这一事实的是__________(填序号)
a. Q单质的熔点比W单质的低
b. W单质的硬度比Q大
c. Q单质能将W从它的盐溶液中置换出来
d. Q的最高价氧化物的水化物的碱性比W的最高价氧化物的水化物的碱性强
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上月考二化学卷(解析版) 题型:选择题
下列说法正确的是( 表示阿伏加德罗常数的值) ( )
表示阿伏加德罗常数的值) ( )
A.1 mol石炭酸 根含有的电子数目为49
根含有的电子数目为49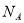
B.标况下1L已烷完全燃烧后恢复至原状态,生成气态物质分子数为6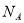 /22.4
/22.4
C.1 mol甲基含有9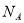 个电子
个电子
D.0.1 mol甘油与足量的钠反应,可生成氢气3.36 L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上月考二化学卷(解析版) 题型:选择题
对于某些离子的检验及结论一定正确的是
A.向某溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32-
B.向某溶液中加入氯化钡溶液有白 色沉淀产生,再加稀硝酸,沉淀不消失,则原溶液中一定有Ag+
色沉淀产生,再加稀硝酸,沉淀不消失,则原溶液中一定有Ag+
C.向某溶液中先加入盐酸酸化,没有明显现象,再加入BaCl2溶液,有白色沉淀产生,则原溶液中一定有SO42-
D.向某溶液中加入加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,则原溶液一定有Ba2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上月考二化学卷(解析版) 题型:选择题
下列离子方程式中,正确的是
A.铜跟硝酸银溶液反应:Cu+Ag+= Cu2++Ag
B.小苏打溶液与稀硫酸混合:CO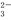 +2H+= CO2↑+H2O
+2H+= CO2↑+H2O
C.大理石溶解于醋酸:CaCO3+2H+= Ca2++CO2↑+H2O
D.CuSO4溶液与Ba(OH)2溶液混合:Cu2++SO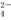 +Ba2++2OH-=BaSO4↓+Cu(OH)2↓
+Ba2++2OH-=BaSO4↓+Cu(OH)2↓
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一12月月考化学试卷(解析版) 题型:实验题
甲同学进行Fe2+还原性的实验,针对异常现象进行探究。
实验:向2 mL FeCl2溶液中滴加2滴0.1 mol•L-1 KSCN溶液,无现象;再滴加5滴5% H2O2溶液(物质的量浓度约为1.5 mol•L-1、pH约为5(酸性环境)),观察到溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2)。
(1)用离子方程式表示实验中溶液变红的原因: 、 。
(2)甲探究实验中溶液褪色的原因:
I.取褪色后溶液两份,一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色;
II.取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀。
III.向2 mL 0.1 mol•L-1 FeCl3溶液中滴加2滴0.1 mol•L-1 KSCN溶液,变红,通入O2,无明显变化。
① 实验I说明 ;②实验III说明 。
得出结论:溶液褪色的原因是酸性条件下H2O2将SCN-氧化成SO42-。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一12月月考化学试卷(解析版) 题型:选择题
向22.4gFe2O3、Cu的混合物中加入0.5 mol·L-1的硫酸溶液600mL时,固体恰好完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
A.6.4g B.4.8g C.2.4g D.1.6g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二12月月考化学试卷(解析版) 题型:填空题
在研究弱电解质的电离、盐类的水解和溶液中离子浓度大小比较中,某师生共同做了这样一个实验:常温下,向20.0mL,0.1mol/L CH3COOH溶液中逐滴加入0.01mol/L NaOH溶液,并在滴加过程中不断用pH计测量混合溶液的pH,绘出pH—V(NaOH)图像,如图所示。请分析:
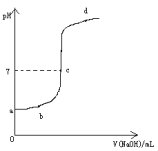
(1)在滴加NaOH溶液至过量过程中的溶液中溶质的变化情况,a、b、c、d各点的溶质各是什么?
(2)CH3COOH与NaOH恰好完全反应的点在图像中的位置在 区域内。(填:pH>7或pH<7或 pH=7),由此可验证CH3COOH为 (填:弱酸或强酸)此时共滴加V(NaOH)= mL。
(3)若将此实验改为中和滴定实验应用 作为指示剂。
(4)随着NaOH的加入,水的电离受到一定的影响,当水的电离达到最大时溶液中的溶质为 。
(5)当测得pH为7时共用去V(NaOH)=VmL,请用V的表达式表示此时CH3COOH的电离平衡常数。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上期末化学试卷(解析版) 题型:实验题
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体 g
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示。
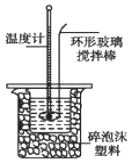
(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol): 。
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
温度 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H= (取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差 ,产生偏差的原因可能是: (填字母)。
,产生偏差的原因可能是: (填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com