
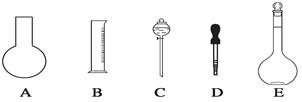
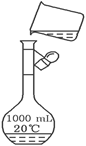
 操作均正确,若定容时俯视视刻度线,则所得溶液浓度_____0.8 mol/L(填“>、<或=”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度_____0.8 mol/L。
操作均正确,若定容时俯视视刻度线,则所得溶液浓度_____0.8 mol/L(填“>、<或=”,下同)。若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度_____0.8 mol/L。 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源:不详 题型:填空题
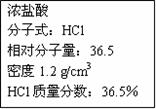  |
| 应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
| | |
 处,改用 加水,使溶液凹面恰好与刻度相切。
处,改用 加水,使溶液凹面恰好与刻度相切。 匀。
匀。 子转移的方向和数目:
子转移的方向和数目:查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 为 mL。
为 mL。 必须选用的仪器有(填序号) ,除此还必需的仪器有
必须选用的仪器有(填序号) ,除此还必需的仪器有  )配制过程中,下列情况会使配制溶液的物质的量浓度偏高的是(填序号)
)配制过程中,下列情况会使配制溶液的物质的量浓度偏高的是(填序号)  线观察液面 ②用量筒取浓硫酸时,仰视读数
线观察液面 ②用量筒取浓硫酸时,仰视读数 中转移溶液时不慎有液滴掉在容量瓶外面 。
中转移溶液时不慎有液滴掉在容量瓶外面 。 用容量瓶前检查它是否漏水
用容量瓶前检查它是否漏水查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 学认为发生双水解反应,其反应方程式为2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3;
学认为发生双水解反应,其反应方程式为2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3; 应选用的试剂是 。
应选用的试剂是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
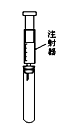
| A.试管中盛酚酞试液,验证氨气的水溶液呈碱性 |
| B.试管中盛酸性高锰酸钾溶液,探究SO2的还原性 |
| C.试管中盛稀氢氧化钠溶液, 验证CO2与NaOH反应的产物 |
| D.装置中充满NO2气体,探究压强对化学平衡的影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 操作 | 可能的实验现象 | 解释 |
| A | 某溶液中加入硝酸酸化的氯化钡溶液 | 有白色沉淀生成 | 溶液中一定含有SO |
| B | 向CaSO3中加入硝酸 | 有刺激性气味的气体生成 | CaSO3与硝酸反应生成SO2 |
| C | 同温同压下用pH试纸测定相同 浓度的碳酸钠和硫酸钠溶液的酸碱性 浓度的碳酸钠和硫酸钠溶液的酸碱性 | 碳酸钠溶液显碱性,硫酸钠溶液显中性 | 碳酸钠溶液发生了水解 |
| D | 向淀粉KI溶液中通入Cl2 | 溶液变蓝 | Cl2与淀粉发生显色反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 .下列对导致这_结果的原因分折中,一定错误的是
.下列对导致这_结果的原因分折中,一定错误的是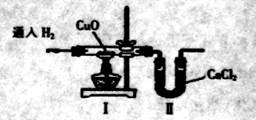
| A.I装置前缺少干燥装置 |
| B.II装置后缺少干燥装置 |
| C.CuO部分被还原成CusO |
| D.通H2前I装置中玻璃管内有水冷凝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 将氯乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验水解产物中的氯离子 |
| B | 向丙醛溶液中加入新制的银氨溶液,用酒精灯直接加热 | 确定丙醛中是否含有醛基 |
| C | 向工业酒精中加入无水硫酸铜 | 确定工业酒精中是否含有水 |
| D | 电石与水反应,制得的气体直接通人酸性KMnO4溶液 | 检验制得的气体是否为乙炔 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com