
| A.浓盐酸 | B.质量分数为70%的H2SO4 |
| C.稀硝酸 | D.质量分数为10%的稀硫酸 |
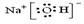 (2) B
(2) B 

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.碱性氢氧燃料电池的正极反应:H2 - 2e- + 2OH-="==" 2H2O |
B.用电子式表示NaCl的形成过程: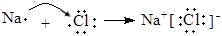 |
| C.向含有Hg2+的废水中加入Na2S可除去Hg2+:Hg2+ + S2- ="==" HgS↓ |
D.汽车尾气系统的催化转化器可降低NO等的排放:2CO+ 2NO 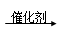 2CO2 +N2 2CO2 +N2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题



查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向AgNO3溶液中滴加氨水至过量:Ag++NH3·H2O=AgOH↓+NH4+ |
| B.向Mg(OH)2悬浊液中滴加FeCl3溶液:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
| C.向Na2S2O3溶液中加入足量稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O |
D.向苯酚钠溶液中通入少量CO2气体: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

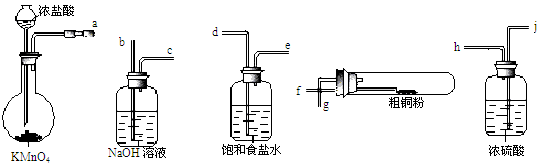
 CuCl42-(aq) + 4 H2O (l)
CuCl42-(aq) + 4 H2O (l)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 离子方程式 | 结论 |
| A | AgCl(s) + I-( aq)  AgI(s) + Cl-(aq) AgI(s) + Cl-(aq) | 溶解度:AgI > AgCl |
| B | Fe2++ H2O2 +2H+= Fe3++2H2O | 氧化性:H2O2 > Fe3+ |
| C | CO32- + CO2 + H2O = 2HCO3- | 稳定性:HCO3- > CO32- |
| D | NH3 + H3O+=NH4++ H2O | 得质子能力:NH3> H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 2SO3(g);△H<0,550 ℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如图所示。
2SO3(g);△H<0,550 ℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如图所示。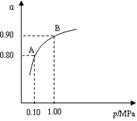
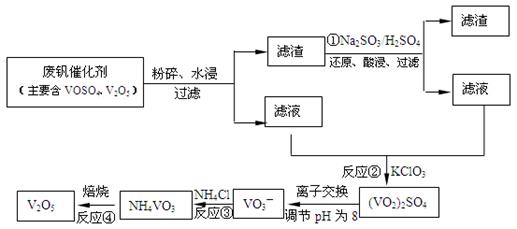
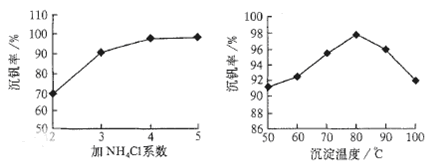
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++H++OH—+SO42—=BaSO4↓+H2O |
| B.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO- |
| C.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4+ |
| D.氯化亚铁溶液中通入氯气:2Fe2++Cl2=2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用烧碱溶液吸收Cl2:Cl2+2OH- =Cl-+ClO-+H2O |
| B.用饱和Na2CO3溶液转化锅垢中的CaSO4:CaSO4(s)+CO32- (aq)=CaCO3(s)+SO42-(aq) |
| C.实验室制备Fe(OH)3胶体:Fe3+ +3OH- =Fe(OH)3↓ |
| D.金属Na与水反应:Na +2H+ = H2↑+Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com