
| ||
| ||


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
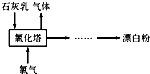 氯气是重要的化工原料.
氯气是重要的化工原料.| C(H+)C(Cl-)C(HClO) |
| C(Cl2) |
| C(H+)C(Cl-)C(HClO) |
| C(Cl2) |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖南省怀化市高一上学期期末考试化学试卷(带解析) 题型:填空题
实验室常用消石灰和NH4Cl固体混合加热制取氨气,回答下列问题:
(1)写出该反应的化学方程式 。
(2)要得到纯净干燥的氨气,可选用的干燥剂是 。
| A.浓硫酸 | B.碱石灰 | C.五氧化二磷 | D.固体NaOH |
查看答案和解析>>
科目:高中化学 来源:2015届湖南省怀化市高一上学期期末考试化学试卷(解析版) 题型:填空题
实验室常用消石灰和NH4Cl固体混合加热制取氨气,回答下列问题:
(1)写出该反应的化学方程式 。
(2)要得到纯净干燥的氨气,可选用的干燥剂是 。
A.浓硫酸 B.碱石灰 C.五氧化二磷 D.固体NaOH
(3)检验氨气常用的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氯气是重要的化工原料.
氯气是重要的化工原料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com