
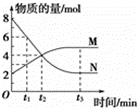
一定温度下,在2L的恒容密闭容器内发生的反应中M、N的物质的量随反应时间变化的曲线如图所示.
请回答下列问题:
(1)该反应的化学方程式为 .
(2)若t2=2min,N的平均反应速率为 .
(3)在t3时刻v正 (填“>”、“<”或“=”)v逆.
考点: 物质的量或浓度随时间的变化曲线;反应速率的定量表示方法.
专题: 化学反应速率专题.
分析: (1)由图可知,N减少,M增加,利用量的变化来分析判断;
(2)根据反应速率v=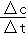 计算;
计算;
(3)t3时刻M、N的物质的量均不再变化,反应达到平衡状态.
解答: 解:(1)由图可知,△n(N)=8mol﹣2mol=6mol,△n(M)=5mol﹣2mol=3mol,N为反应物,M为生成物,变化量之比为2:1,即化学计量数之比为2:1,反应为2N⇌M;
故答案为:2N⇌M;
(2)t2=2min,N的平均反应速率v=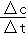 =
=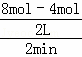 =1mol•L﹣1•min﹣1;
=1mol•L﹣1•min﹣1;
故答案为;1mol•L﹣1•min﹣1;
(3)t3时刻M、N的物质的量均不再变化,反应达到平衡状态,故v正=v逆.
故答案为:=.
点评: 本题考查了根据图象计算化学反应速率、判断化学平衡状态的问题,难度不大,注意把握图象的分析.


科目:高中化学 来源: 题型:
下列叙述正确的是()
A. 工业上电解熔融的Al2O3冶炼铝用铁做阳极
B. 用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1:2
C. 用惰性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1mol NaOH
D. 用惰性电极电解浓CuSO4溶液一小段时间后,加入Cu2O固体可以使CuSO4溶液恢复原来浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,浓度都是1mol•L﹣1的两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得物质的浓度分别为c(X2)=0.6mol•L﹣1,c(Y2)=0.8mol•L﹣1,c(Z)=0.4mol•L﹣1,则该反应的反应式可表示为()
A. X2+2Y2═2XY2 B. 2X2+Y2═2X2Y C. 3X2+Y2═2X3Y D. X2+3Y2═2XY3
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H﹣H键的键能为436kJ/mol,O═O键的键能为498kJ/mol,根据热化学方程式H2(g)+ O2(g)═H2O(l)△H=﹣286kJ/mol,判断H2O分子中O﹣H键的键能为()
O2(g)═H2O(l)△H=﹣286kJ/mol,判断H2O分子中O﹣H键的键能为()
A. 485.5 kJ/mol B. 610 kJ/mol C. 917 kJ/mol D. 1 220 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式C2H2(g)+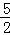 O2(g)═2CO2(g)+H2O(g)△H=﹣1256kJ/mol,下列说法正确的是()
O2(g)═2CO2(g)+H2O(g)△H=﹣1256kJ/mol,下列说法正确的是()
A. 乙炔(C2H2)的燃烧热为1256 kJ/mol
B. 若转移10 mol电子,则消耗2.5 mol O2
C. 若生成2 mol液态水,则△H=﹣2512 kJ/mol
D. 若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
在微生物作用下,NH4+经过两步反应被氧化成NO3﹣.反应的能量变化示意图如下:
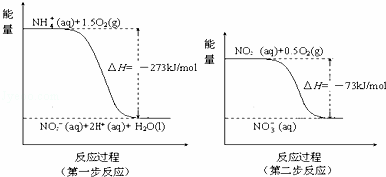
①第一步反应是 反应(选填“放热”或“吸热”),判断依据是 .
②1mol NH4+(aq)全部氧化成NO3﹣(aq)的热化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池.①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少.据此判断这四种金属活泼性由大到小的顺序是()
A. ①③②④ B. ①③④② C. ③④②① D. ③①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,摩托罗拉公司开始了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月.如图是一个电化学过程的示意图.已知甲池总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O
2K2CO3+6H2O
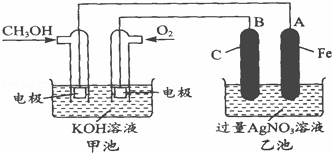
请填空:
(1)充电时:①原电池的负极与电源负极相连.②阳极的电极反应式为
(2)放电时,负极的电极反应式为
(3)在此过程中若完全反应,乙池中A极的质增加648g,则甲池中理论上消耗O2 L(标准状况下).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于钠的说法正确的是()
A. 金属钠与少量氧气反应生成氧化钠,与足量氧气反应生成过氧化钠
B. 钠的化学 性质活泼,可从CuSO4溶液中置换出Cu
性质活泼,可从CuSO4溶液中置换出Cu
C. 钠着火时可以用沙土盖灭
D. 钠在空气中燃烧,产生黄色火花
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com