
| 3g |
| 30g/mol |


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
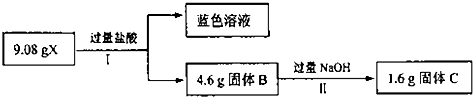
 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某不同品牌铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某不同品牌铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.| 盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、美丽的“水立方”是北京奥运会游泳馆,设计灵感来自于有机细胞的天然图案以及肥皂泡的形成.在这个中心的蓝色泡墙之内,钢结构的基本单位是一个由12个正五边形和2个正六边形组成的几何细胞,覆盖这个框架的是半透明的“气泡”,称为ETFE,该材料为四氟乙烯(CF2=CF2)与乙烯的共聚物,ETFE属于有机物中的烃类. |
| B、5月12日四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒剂、漂白剂,如:Ca(ClO)2、ClO2、Al(OH)3等. |
| C、美国科学家马丁?查非(Martin Chalfie)、美国华裔化学家钱永健(Roger Tsien)以及日本科学家下村修(Osamu Shimomura)因发现和研究绿色荧光蛋白(green fluorescent protein,GFP)而获2008年度诺贝尔化学奖.向GFP中加入重金属离子,GFP就会变性. |
| D、神舟七号载人飞船于2008年9月25日21点10分发射升空.中国航天员首次空间出舱活动.“神舟七号”的燃料是氢化锂三兄弟--LiH、LiD、LiT.其中Li的质量数为7,这三种物质的化学性质不相同. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向明矾溶液中加入等物质的量的Ba(OH)2溶液Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| B、向Fe2(SO4)3溶液中通入足量的H2S:Fe3++H2S=Fe2++S↓+2H+ |
| C、向硝酸银溶液中滴加过量氨水:Ag++2NH3?H2O=[Ag(NH3)2]++2H2O |
| D、含等物质的量的硫酸氢铵与氢氧化钠两种溶液混合:NH4++HSO4-+2OH-=SO42-+NH3↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠着火时可用干粉灭火器扑灭 |
| B、在硫酸铜晶体结晶水含量测定的实验中,称量操作至少需要四次 |
| C、铜与浓硫酸反应时,用蘸有浓溴水的棉花放在导管口吸收多余的气体 |
| D、在250 mL烧杯中加入216 mL水和24 g NaOH固体,配制10%NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,下列说法中错误的是( )
,下列说法中错误的是( )| A、X可以是金属 |
| B、X可以是非金属 |
| C、m可以等于1或2 |
| D、XYm与XYn的相互转化是可逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将氨水逐滴滴加到AlCl3溶液中:Al3++3OH-=Al(OH)3↓ |
| B、铜与稀硝酸反应:Cu+4H++NO3-=Cu2++NO↑+2H2O |
| C、硫酸与氢氧化钡在溶液中反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、用FeCl3溶液腐蚀铜箔制造的印刷电路板:2Fe3++Cu=2Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
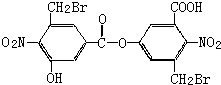
| A、该有机物的分子式为:C16H9O8N2Br2 |
| B、向该有机物溶液中加入FeCl3溶液,振荡后有紫色沉淀产生 |
| C、1mol该有机物与足量的NaOH溶液混合共热,充分反应最多可消耗6 mol NaOH |
| D、该有机物在稀硫酸中加热水解,有机产物只有一种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com