
 =3n对,根据n=
=3n对,根据n= 计算14gCnH2n的物质的量,再根据N=nNA计算共用电子对数.
计算14gCnH2n的物质的量,再根据N=nNA计算共用电子对数. 计算氨气的物质的量,根据氮原子守恒可知,溶液中氮原子数目等于11.2LNH3含有的氮原子数目.
计算氨气的物质的量,根据氮原子守恒可知,溶液中氮原子数目等于11.2LNH3含有的氮原子数目. =
=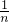 mol,每个CnH2n分子中含有共用电子对为3n对,所以,14gCnH2n中含有的共用电子对数为3NA,故B错误;
mol,每个CnH2n分子中含有共用电子对为3n对,所以,14gCnH2n中含有的共用电子对数为3NA,故B错误;

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com