
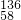 Ce、
Ce、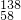 8Ce、
8Ce、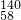 Ce、
Ce、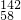 Ce,它们互为同位素
Ce,它们互为同位素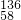 Ce、
Ce、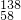 8Ce、
8Ce、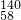 Ce、
Ce、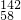 Ce中,具有相同质子数,不同中子数,故它们互为同位素,故B正确;
Ce中,具有相同质子数,不同中子数,故它们互为同位素,故B正确;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011届重庆市重庆一中高三3月月考(理综)化学部分 题型:单选题
稀土是工业味精,邓小平说过“中东有石油,我们有稀土”。金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是
| A.电解熔融CeO2制Ce,铈在阳极获得 |
B.铈有四种稳定的核素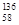 Ce、 Ce、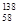 Ce、 Ce、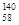 Ce、 Ce、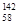 Ce,它们互为同素异形体 Ce,它们互为同素异形体 |
| C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+ |
| D.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑ |
查看答案和解析>>
科目:高中化学 来源:2010-2011学年重庆市高三3月月考(理综)化学部分 题型:选择题
稀土是工业味精,邓小平说过“中东有石油,我们有稀土”。金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是
A.电解熔融CeO2制Ce,铈在阳极获得
B.铈有四种稳定的核素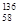 Ce、
Ce、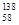 Ce、
Ce、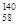 Ce、
Ce、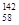 Ce,它们互为同素异形体
Ce,它们互为同素异形体
C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+
D.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑
查看答案和解析>>
科目:高中化学 来源:2014届河北正定中学高一下学期第1次考试化学试卷 题型:选择题
稀土是工业味精,邓小平说过“中东有石油,我们有稀土”。稀土元素铈(Ce)主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是( )
A.已知Ce原子序数是58,则其为镧系元素
B.铈有四种稳定的核素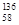 Ce、
Ce、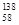 Ce、
Ce、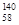 Ce、
Ce、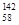 Ce,它们互为同位素
Ce,它们互为同位素
C.用Ce(SO4)2溶液可与硫酸亚铁溶液反应,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+
D.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑
查看答案和解析>>
科目:高中化学 来源:2013届河北省高一下学期第一次月考化学试卷 题型:选择题
稀土是工业味精,邓小平说过“中东有石油,我们有稀土”。稀土元素铈(Ce)主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是
A.已知Ce原子序数是58,则其为镧系元素
B.铈有四种稳定的核素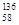 Ce、
Ce、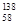 8Ce、
8Ce、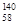 Ce、
Ce、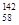 Ce,它们互为同位素
Ce,它们互为同位素
C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+
D.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com