(2011?枣庄模拟)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
(1)常温下,某氨水的pH=12,则水电离的c(OH
-)=
1×10-12mol/L
1×10-12mol/L
.若向该氨水中加入等体积、等物质的量浓度的盐酸,此时溶液中水电离的程度
大于
大于
(填“大于”、“等于”或“小于”)氨水中水的电离程度.
(2)合成氨反应N
2(g)+3H
2(g)?2NH
3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡
向左
向左
移动(填“向左”、“向右”或“不”).
(3)一定温度下,在密闭容器中可发生下列反应:2N
2O
5(g)?4NO
2(g)+O
2(g).下表为反应在T
1温度下的部分实验数据:
| T/s |
0 |
500 |
1000 |
| c(N2O5)/mol?L-1 |
5.00 |
3.50 |
2.42 |
则500s内N
2O
5的分解速度v(N
2O
5)=
3×10-3mol?L-1?s-1
3×10-3mol?L-1?s-1
;降温至T
2,反应进行1000s时测得c(NO
2)=4.98mol?L
-1,则反应
N
2O
5(g)?NO
2(g)+O
2(g)的△H
<
<
0.(填“>”、“=”、“<”).
(4)最近美国Simons等科学家发明了使NH
3直接用于燃料电池的方法,其装置用铂黑作电极、加入电解质溶液中,一个电极通入空气,另一电极通入NH
3.其电池反应式为:4NH
3+3O
2═2N
2+6H
2O.你认为电解质溶液应显
碱性
碱性
(填“酸性”、“中性”或“碱性”),写出正极的电极反应方程式
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.

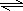 H++OH-计算;先根据氨水抑制了水的电离,氨水与等体积、等物质的量浓度的盐酸反应生成氯化铵,氯化铵水解促进了水的电离;
H++OH-计算;先根据氨水抑制了水的电离,氨水与等体积、等物质的量浓度的盐酸反应生成氯化铵,氯化铵水解促进了水的电离;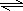 H++OH-,
H++OH-,

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案 2SO3(g)△H=-196.6KJ?mol- 1)
2SO3(g)△H=-196.6KJ?mol- 1)