




 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
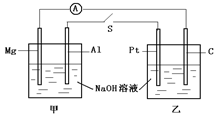
| A.电流计指针不发生偏转 |
| B.Al、Pt两电极有氢气生成 |
| C.甲池pH减小,乙池pH不变 |
| D.Mg、C两电极生成的气体在一定条件下可恰好完全反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
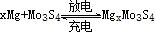 ,下列说法不正确的是( )
,下列说法不正确的是( )| A.放电时,正极反应式:Mo3S4+2xe- =Mo3S42x- |
| B.放电时,Mo3S4发生氧化反应 |
| C.充电时,Mg2+向阴极迁移 |
| D.充电时,阴极反应式:xMg2++2xe-=xMg |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
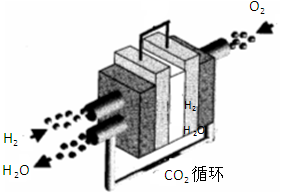
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Fe(OH)2 + Ni(OH)2。
Fe(OH)2 + Ni(OH)2。| A.NiO2 | B.Fe | C.Fe(OH)2 | D.Ni(OH)2 |
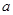 g M,则金属M的相对原子质量为 (用含“
g M,则金属M的相对原子质量为 (用含“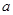 、x”的表达式表示)。
、x”的表达式表示)。 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B.设想把“H2+Cl2===2HCl”设计成燃料电池,用于工业制盐酸,并进行发电 |
| C.纯锌与稀硫酸反应产生氢气的速率较慢,再加入少量CuSO4固体,速率不变 |
| D.原电池的两极一定是由活泼性不同的两种金属组成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属腐蚀的本质是金属原子失去电子而被氧化 |
| B.金属腐蚀一般包括化学腐蚀和电化学腐蚀 |
| C.纯的金属一般难以发生电化学腐蚀 |
| D.镀锌铁当镀层破损后,镀层则对铁失去了保护作用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
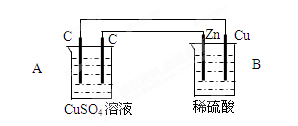
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com