
能用H+ + OH- = H2O表示的是 ( )
A.Ba(OH)2溶液和稀H2SO4的反应
B.Cu(OH)2和稀H2SO4的反应
C.NaOH溶液和氢溴酸反应
D.NaOH溶液和醋酸溶液的反应
科目:高中化学 来源:2016届云南玉溪第一中学高三上学期期中考试理化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法正确的是( )
A、纤维素在人体内可水解为葡萄糖,故可做人类的营养物质
B、煤经过气化和液化等物理变化可以转化为清洁燃料
C、侯氏制碱法的工艺过程中应 用了物质溶解
用了物质溶解 度的差异
度的差异
D、用硫酸清洗锅炉中的水垢
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上学期12月第四次月考化学试卷(解析版) 题型:选择题
下列反应中,有沉淀产生且不会消失的是 ( )
A.向NaOH溶液中逐滴滴入Fe2(SO4)3溶液直至过量
B.将NaOH溶液逐滴滴入AlCl3溶液中,直至过量
C.向AlCl3溶液中逐滴滴入稀硫酸
D.将氨水逐滴滴入硝酸银溶液中,直至过量
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.C02分子的比例模型:
B.过氧化氢的电子式:H: O:O:H
C.氟原子的结构示意图: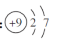
D. H2CO3 的电离方程式:H2CO3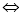 2H+ +CO32-
2H+ +CO32-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高一上期中化学试卷(解析版) 题型:计算题
常温下,在35.5g水中溶解12.5g CuSO4·5H2O,恰好达到饱和,该溶液密度为1.20g /cm3,求:(1)该溶液中阴阳离子的总物质的量;
(2)该溶液中CuSO4的物质的量浓度;
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期12月月考化学试卷(解析版) 题型:填空题
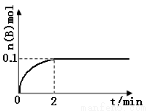
(1)在一定温度下,向1L体积固定的密闭容器中加入1molA(g),发生反应2A(g) B(g)+C(g),B的物质的量随时间的变化如图所示。 0—2min内的平均反应速率v(A)= . 相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时 是原来的2倍。
B(g)+C(g),B的物质的量随时间的变化如图所示。 0—2min内的平均反应速率v(A)= . 相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时 是原来的2倍。
a.平衡常数 b.A的平衡浓度 c.达到平衡的时间
d.平衡时B的体积分数 e.平衡时混合气体的密度
f .平衡时混合气体的平均摩尔质量
(2)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡 移动(填“向左”“向右”或“不”);若加入少量下列试剂中的 ,产生H2的速率
将增大。
a.NaNO3 b.CuSO4 c.Na2SO4 d.NaHSO3 e. CH3COOH f.FeSO4
(3)用惰性电极电解Cu(NO3)2 溶液一段时间后,加入a mol 的Cu(OH)2可使溶液恢复原状,则电解过程中转移的电子数目为_____________
(4)氯化铁溶液常作印刷电路铜板的腐蚀剂,得 到含有Cu2+等的废液,有人提出可以利用如右图的装置从得到的废液中提炼金属铜。该过程中甲池负极的电极反应式是 ,若乙池中装入废液500mL,当阴极增重3.2g时,停止通电,此时阳极产生气体的体积(标准状况)为 (假设气体全部逸出)。

查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三上学期12月月考理综化学试卷(解析版) 题型:填空题
工业生产硝酸铵的流程如下图所示
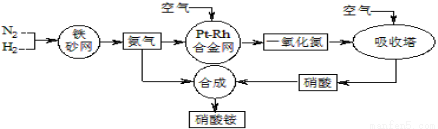
(1)硝酸铵的水溶液呈 (填“酸性”、“中性”或“碱性”);其水溶液中各离子的浓度大小顺序为: 。
(2)已知N2(g)+3H2(g) 2NH3(g) △H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如右图。
2NH3(g) △H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如右图。
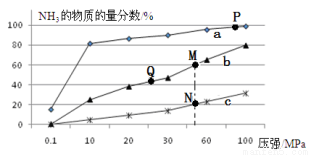
①曲线a对应的温度是 。
②关于工业合成氨的反应,下列叙述正确的是
A.及时分离出NH3可以提高H2的平衡转化率
B.P点原料气的平衡转化率接近100%,是当前工业生产工艺中采用的温度、压强条件
C.上图中M、N、Q点平衡常数K的大小关系是K(M)=K(Q)>K(N)
D.M点比N点的反应速率快
E.如果N点时c(NH3)=0.2 mol·L-1,N点的化学平衡常数K≈0.93
(3)尿素(H2NCONH2)是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为二步反应:
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272 kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138 kJ·mol-1
写出工业上以NH3、CO2为原料合成尿素的热化学方程式: ;
(4)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如下左图所示:
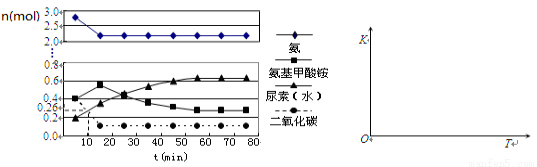
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_____步反应决定,总反应进行到_________min时到达平衡。
②在上右图中画出第二步反应的平衡常数K随温度的变化的示意图。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上第三次模拟化学试卷(解析版) 题型:选择题
室温下,下列各组离子在指定溶液中能大量共存的是( )
A.(NH4)2Fe(SO4)2溶液中:Ba2+、K+、OH-、Br-
B.通入过量SO2气体的溶液中:H+、Ba3+、NO3-、Fe3+
C.c(OH-)/c(H+)=10-12的溶液中:NH4+、Cu2+、NO3-、Cl-
D.c(I-)=0.1mol/L的溶液中:Na+、Fe3+、ClO-、SO42-
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰二中高三上学期12月月考理综化学试卷(解析版) 题型:选择题
化学与社会、技术、环境、生活密切相关。下列说法正确的是( )
A.碘是人体必需的微量元素,所以要多吃富含高碘酸的食物
B.空气中直径小于或等于2.5?m的颗粒物称为PM2.5
C.pH<7的雨水称为酸雨,对环境造成很大的危害
D.甲醛的水溶液可以作为鱿鱼等海鲜的防腐剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com