
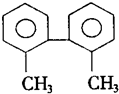
| A. | 分子中至少有8个碳原子处于同一平面上 | |
| B. | 分子中至少有9个碳原子处于同一平面上 | |
| C. | 该烃的一氯取代物最多有8种 | |
| D. | 该烃是苯的同系物 |
分析 A、B可根据苯环的结构判断;
C.根据等效氢原子判断同分异构体;
D.苯的同系物指含有1个苯环,侧链为烷基.
解答 解:A、B.甲基与苯环平面结构通过单键相连,甲基的C原子处于苯的H原子位置,所以处于苯环这个平面.两个苯环相连,与苯环相连的碳原子处于另一个苯的H原子位置,也处于另一个苯环这个平面,另一苯环所用的C原子都处于同一平面上,至少有1个碳原子与另一个苯环同平面,所以至少有9个碳原子共面,故A错误、B正确;
C.每个苯环上4个H各不相同,取代苯环上的H有4种异构体,再加上甲基被取代,则该烃的一氯取代物最多有5种,故C错误;
D.该有机物含有2个苯环,与苯在组成上不相差-CH2的倍数,且不饱和度不同,不是苯的同系物,故D错误;
故选B.
点评 本题主要考查有机化合物的结构特点,为高频考点,侧重于学生的分析能力的考查,题目难度中等,易错点为B、C,注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构.


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:选择题
| A. | Fe+CuSO4=FeSO4+Cu | B. | Cl2+H2O=HCl+HClO | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | AgNO3+HCl=AgCl↓+HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .化合物
.化合物 是合成药物的中间体,请写出以有机物A和
是合成药物的中间体,请写出以有机物A和 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸和NaOH溶液反应 | B. | 氯化氢溶于水 | ||
| C. | 稀硫酸与BaCl2溶液反应 | D. | 氯化氢与氨气反应生成NH4Cl固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com