
下列现象或事实可用同一原理解释的是 ( )
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低
B.SO2和FeSO4溶液使酸性高锰酸钾的紫色褪去
C.漂白粉和水玻璃长期暴露在空气中变质
D.亚硫酸钠溶液和氯化铝溶液在空气中蒸干不能得到对应的溶质
科目:高中化学 来源: 题型:
某有机物的结构简式为  ,它可以发生的反应类型有
,它可以发生的反应类型有
①加成 ②消去 ③水解 ④酯化 ⑤氧化 ⑥加聚
A.①②③④ B.①②④⑤ C.①②⑤⑥ D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。
(1)写出基态Mn原子的外围电子排布式 。在 Mn的基态原子中有 种能量不同的电子。
(2)CoTiO3晶体结构模型如图1所示。在CoTiO3晶体中1个Ti原子、1个Co原子,周围距离最近的O原子数目分别为 个、 个。
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂, 常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO- 互为等电子体的分子、离子化学式分别为 、 (各写一种)。
(4)三聚氰胺是一种含氮化合物,其结构简式如图2所示。

三聚氰胺分子中氮原子轨道杂化类型是 , 1 mol三聚氰胺分子中 σ键的数目为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
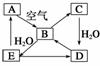 图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条
图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条
件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4∶5,化合物D是重要的工业原料。
(1)写出A在加热条件下与H2反应的化学方程式:
________________________________________________________________________;
(2)写出E与A的氢化物反应生成A的化学方程式:
________________________________________________________________________;
(3)写出一个由D生成B的化学方程式:
________________________________________________________________________;
(4)将5 mL 0.10 mol·L-1的E溶液与10 mL 0.10 mol·L-1的NaOH溶液混合。
①写出反应的离子方程式:________________________________________________;
②反应后溶液的pH________7(填“大于”、“小于”或“等于”),理由是________________________________________________________________________;
③加热反应后的溶液,其pH________(填“增大”、“不变”或“减小”),理由是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要。完成下列填空:
(1)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。
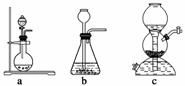
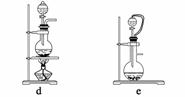
如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置是________(填写字母)。
(2)若用硫酸和亚硫酸钠反应制取3.36 L(标准状况)二氧化硫,至少需要称取亚硫酸钠________g(保留一位小数);如果已有40%亚硫酸钠(质量分数)被氧化成硫酸钠,则至少需称取该亚硫酸钠________g (保留一位小数)。
(3)实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通。石灰石膏法和碱法是常用的烟气脱硫法。
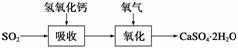
石灰石膏法的吸收反应为SO2+Ca(OH)2―→CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O―→2CaSO4·2H2O。其流程如下图:
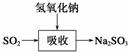
碱法的吸收反应为SO2+2NaOH―→Na2SO3+H2O。碱法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如下图:
已知:
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.9 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
石灰石膏法和碱法吸收二氧化硫的化学原理相同之处是
________________________________________________________________________。
和碱法相比,石灰-石膏法的优点是_______________________________________,
缺点是__________________________________________________________________。
(4)在石灰石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
研究性学习小组做铜与浓硫酸反应的实验时,发现试管底部有白色固体并夹杂有少量黑色物质。倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有少量水的烧杯中,发现所得溶液为蓝色,黑色固体未溶解。过滤、洗涤后,向黑色固体中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,向所得溶液中加BaCl2溶液后有白色沉淀生成。下列结论不正确的是 ( )
A.铜与浓硫酸反应所得白色固体是CuSO4
B.加BaCl2溶液后所得白色沉淀是BaSO4
C.白色 固体中夹杂的少量黑色物质可能是CuO
固体中夹杂的少量黑色物质可能是CuO
D.白色固体中夹杂的少量黑色物质中含元素Cu、S
查看答案和解析>>
科目:高中化学 来源: 题型:
国际纯粹与应用化学联合会(IUPAC)将117号元素暂时命名为Uus,以下关于Uus的叙述正确的是
A.是稀有气体 B.有放射性 C.是第六周期元素 D.质量数为117
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是
A.MnO2 与浓盐酸反应制Cl2:MnO2+4HCl Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
B.铜与稀硝酸反应:Cu+4H++2NO3- === 2H2O +Cu2++2NO2↑
C.足量氨水吸收少量二氧化硫气体:NH3·H2O+SO2=NH4++HSO3-
D.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3- +Ca2++OH-=== CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
由短周期元素构成的某离子化合物X中,一个阳离子和一个阴离子核外电子数之和为20,则有关X的下列说法中正确的是( )
A.X中阳离子和阴离子个数不一定相等
B.X中一定有离子键,一定不含共价键
C.若X只含两种元素,则这两种元素可在同一周期也可在同一主族
D.X中阳离子半径一定大于阴离子半径
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com