分析:该原电池中,锌易失电子发生氧化反应而作负极,铜作正极,正极上铜离子得电子发生还原反应,在得失电子相等的条件下,将正负极电极反应式相加即得电池反应式.
解答:解:(1)该原电池中,锌易失电子作负极,铜作正极,正极上铜离子得电子生成铜单质Cu2++2e-=Cu,所以正极上看到的现象是:铜片上有红色的铜析出;
故答案为:正;有红色的铜析出;Cu2++2e-=Cu;
(2)锌易失电子生成锌离子而作负极,电极反应式为:Zn-2e-=Zn2+,故答案为:负;Zn-2e-=Zn2+;
(3)在得失电子相等的条件下,将正负极电极反应式相加即得电池反应式,所以电池反应式为Cu2++Zn=Zn2++Cu,故答案为:Cu2++Zn=Zn2++Cu.
点评:明确原电池的工作原理及所发生的氧化还原反应是解答本题的关键,难度不大.

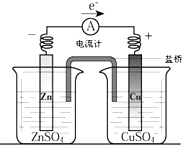 如图为铜锌原电池的装置请回答:
如图为铜锌原电池的装置请回答:
