
 高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )
高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )| A. | 铁是阳极,电极反应为 Fe-6e-+4H2O=FeO42-+8H+ | |
| B. | 电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 | |
| C. | 若隔膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO42- | |
| D. | 电解时阳极区pH 降低、阴极区 pH升高,撤去隔膜混合后,与原溶液比较 pH升高(假设电解前后体积变化忽略不计) |
分析 A、依据装置图分析可知铁与电源正极相连做电解池阳极,碱性溶液不能生成氢离子;
B、电解过程中电子流向负极流向Ni电极,不能通过电解质溶液,是通过电解质溶液中离子定向移动实现闭合电路,通过Fe电极回到正极;
C、阴离子交换膜只允许阴离子通过;阴离子移向阳极,若离子交换膜为阴离子交换膜,电解结束后由于浓度差左侧溶液中会含有FeO42-;
D、阳极区域,铁失电子消耗氢氧根离子,溶液pH减小,阴极区氢离子得到电子生成氢气,溶液中氢氧根离子浓度增大,溶液pH增大;依据电子守恒分析生成氢氧根离子和消耗氢氧根离子相对大小分析溶液酸碱性.
解答 解:A、依据装置图分析可知铁与电源正极相连做电解池阳极,碱性溶液不能生成氢离子,电极反应为Fe-6e-+8OH-═FeO42-+4H2O,故A错误;
B、电解过程中电子流向负极流向Ni电极,不能通过电解质溶液,是通过电解质溶液中离子定向移动实现闭合电路,通过Fe电极回到正极,故B错误;
C、阴离子交换膜只允许阴离子通过,阴离子移向阳极,应从左向右移动,若离子交换膜为阴离子交换膜,则电解结束后由于浓度差左侧溶液中会含有FeO42-,故C正确;
D、阳极区域,铁失电子消耗氢氧根离子,溶液PH减小,阴极区氢离子得到电子生成氢气,溶液中氢氧根离子浓度增大,溶液PH增大;生成氢氧根离子物质的量消耗,在阳极电极反应Fe-6e-+8OH-═FeO42-+4H2O,阴极氢氧根离子增大,电极反应2H++2e-=H2↑,依据电子守恒分析,氢氧根离子消耗的多,生成的少,所以溶液pH降低,故D错误;
故选C.
点评 本题考查了电解原理,正确判断阴阳极及发生的反应是解本题关键,易错选项是B,注意电子不能通过电解质溶液,题目难度中等.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 30mL | B. | 40mL | C. | 50mL | D. | 60mL |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
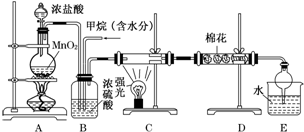
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中滴加氯水,再滴加KSCN溶液,若溶液变成血红色,则原溶液中一定有Fe2+ | |
| B. | 钾元素焰色反应的操作是:将铂丝放在稀盐酸中洗涤后灼烧至无色,然后再用铂丝蘸取固体氯化钾,进行灼烧,直接观察火焰颜色 | |
| C. | 向某溶液中滴加氯化钡溶液,产生白色沉淀,再滴加足量稀硝酸,依然有白色固体,说明原溶液含有SO42- | |
| D. | 向某黄色溶液中加入淀粉溶液,若溶液变蓝色,则原溶液中含有I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤⑥ | B. | ①②④⑤ | C. | ②③⑤⑥ | D. | ③④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液、盐酸、氨气 | B. | 硫酸、NaOH溶液、盐酸 | ||
| C. | NaOH溶液、盐酸、CO2 | D. | 水、盐酸、NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2(CaO):HCl | B. | MgO(Al2O3):NaOH | C. | CO2(SO2):Ca(OH)2 | D. | NaCl(NH4Cl):加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
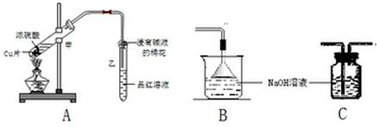
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅含碳、氢元素的有机物称为烃 | |
| B. | 1,2-二溴乙烷是无色液体 | |
| C. | 溴苯的密度比水大 | |
| D. | 四氟乙烯(CF2=CF2)中含有碳碳双键,属于烯烃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com