
下列离子方程式的书写正确的是( )
| A.实验室用大理石和稀盐酸制取CO2:2H+ + CO32-= CO2 + H2O |
| B.铁和稀硫酸反应:Fe + 2H+= H2 + Fe3+ |
| C.NH4HCO3溶液中加入过量的NaOH溶液:NH4+ + OH-= NH3+H2O |
| D.NaHCO3溶液与NaOH溶液反应:OH- + HCO3-= CO32- + H2O |
D
解析试题分析:A. 大理石难溶,不能写成离子形式。正确的写法为: 实验室用大理石和稀盐酸制取CO2:2H+ + CaCO3 = Ca2++CO2 + H2O。错误。B. 稀硫酸的氧化性弱,只能把Fe氧化为Fe2+。离子方程式为:Fe + 2H+ =H2 + Fe2+.错误。C. NH4HCO3溶液中加入过量的NaOH溶液OH-既可以与NH4+反应也可以与HCO3-反应,而且在没有加热时NH3·H2O不能写成分解产物的形式。离子方程式为:NH4+ +2 OH- +HCO3-= CO32-+ H2O +NH3·H2O 。错误。D.符合离子方程式书写原则。正确。
考点:考查离子方程式的书写的知识。


科目:高中化学 来源: 题型:单选题
在碱性溶液中能够大量共存且溶液为无色透明的离子组是
| A.Na+ NH4+ NO3- Cl- | B.Na+ K+ CO32- NO3- |
| C.K+ Ba2+ HCO3- Cl- | D.Na+ K+ MnO4- SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子能在溶液中大量共存,当将溶液的pH调节至1时就会出现浑浊的是
| A.Fe2+、Fe3+、NH4+、NO3- | B.S2-、K+、I-、SO32- |
| C.Na+、I-、CO32-、NO3- | D.Al3+、HCO3-、OH-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是
| A.固体氯化钠不导电,所以氯化钠不是电解质 |
| B.铜丝能导电,所以铜是电解质 |
| C.氯化氢水溶液能导电,所以氯化氢是电解质 |
| D.SO3 溶于水能导电,所以 SO3 是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入过量的CO2
②向Fe(OH)3胶体中逐滴加入过量的稀盐酸
③向NaAlO2溶液中通入过量的CO2
④向澄清石灰水中通入缓慢过量的CO2
| A.①② | B.①④ | C.①③ | D.②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组离子在溶液中能大量共存的是
A.Na+、Al3+、Cl-、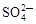 | B.Cu2+、Cl-、 、OH- 、OH- |
C.Ca2+、Na+、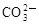 、 、 | D.H+、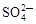 、 、 、OH- 、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
能正确表示下列反应的离子反应方程式为
| A.NH4HCO3溶于过量的浓KOH溶液中:NH4++ OH-= NH3↑+ H2O |
| B.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -="2" Al(OH)3↓+3BaSO4↓ |
| C.向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2="2" Fe3++2 Br2+6 Cl- |
| D.醋酸除去水垢:2H++CaCO3=Ca2++ CO2↑+ H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温,下列各组离子在指定溶液中能大量共存的是( )
| A.pH=1的溶液中: I-、NO3-、SO42-、Na+ |
| B.由水电离的c(H+)=1×10-14 mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的溶液中: NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)="0.1" mol·L-1的溶液中:K+、ClO-、SO42-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某无色溶液中可能含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO32-、⑥SO42-离子中的若干种,依顺序进行下列实验,且每步所加试剂均过量,观察到的现象如下:
| 步骤 | 操作 | 现象 |
| 1 | 用pH试纸检验 | 溶液的pH大于7 |
| 2 | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
| 3 | 分液,向上层溶液中加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| 4 | 过滤,向滤液中加入AgNO3溶液 | 有白色沉淀产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com