
 OH
OH科目:高中化学 来源:不详 题型:单选题
| A.电解质溶液中混入水,对电池反应无影响 |
| B.上述过程中是电能转化成化学能 |
| C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3 |
| D.电池工作过程中,金属锂提供电子的物质的量与析出硫的物质的量之比为4 :1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
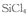 也可转化为
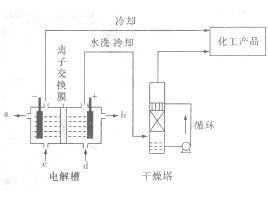
也可转化为 而循环使用。一定条件下,在200C恒容密闭容器中发生反应:
而循环使用。一定条件下,在200C恒容密闭容器中发生反应: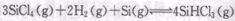 ,达平衡后,H2与SiHCL3物质的量浓度分别为0. 140mol/L和0. 020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的物质的量为_______ (2分)mol。
,达平衡后,H2与SiHCL3物质的量浓度分别为0. 140mol/L和0. 020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的物质的量为_______ (2分)mol。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
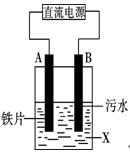
| A.与电源正极相连的是电解槽的阴极。 | B.与电源负极相连的是电解槽的负极。 |
| C.电解槽的阳极发生还原反应。 | D.电子从电源的负极沿导线流入电解槽的阴极。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
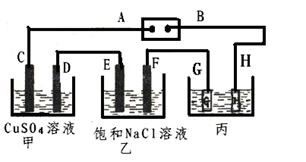
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
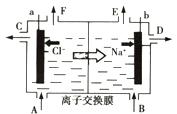
| A.从E口逸出的是氢气 |
| B.向B口中加入含少量NaOH 的溶液以增强导电性 |
| C.标准状况下每生成22.4LCl2,便产生2molNaOH |
| D.向电解后的阳极室溶液中加入适量盐酸,各物质可以恢复到电解前的浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 电的离子数目比为2:1,可供选择的电解液有下列四组,则符合题意的为哪一组?
电的离子数目比为2:1,可供选择的电解液有下列四组,则符合题意的为哪一组?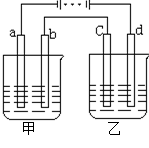
| | A | B | C | D |
| 甲 | AgNO3 | NaCl | K2S | KOH |
| 乙 | CuCl2 | CuSO4 | H2SO4 | AgNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用明矾净水是因为Al2+水解生成的Al(OH)3胶粒具有很强的吸附性 |
| B.合成氨生成过程中,采用高温高压都是为了提高N2、H2转化率 |
| C.往铁钉镀铜时,用铜做阴极 |
| D.电解饱和食盐水制烧碱,NaOH在阳极区域产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com