


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:022
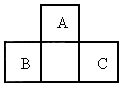
A、B、C均为短周期元素,它们在周期表中的位置如图所示.已知B、C两元素原子的最外层电子数之和等于A元素原子最外层电子数的2倍;B、C两元素的原子序数之和是A元素序数的4倍.则A、B、C的元素符号分别为________,________,________;元素名称分别为________,________,________;B、C两种元素最高价氧化物对应水化物的酸性或碱性的强弱顺序为________.

查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
A、B、C均为短周期元素,它们在周期表中的位置如右面所示.已知B、C两元素原子的最外层电子数之和等于A元素原子最外层电子数的2倍;B、C两元素的原子序数之和是A元素序数的4倍.则A、B、C的元素符号分别为________,_________,_________;元素名称分别为__________,_________,___________;B、C两种元素最高价氧化物对应水化物的酸性或碱性的强弱顺序为____________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com