
【题目】某温度时,在2 L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
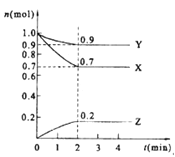
(1)由图中所给数据进行分析,该反应的化学方程式为 ;
(2)反应从开始至2分钟,用Z的浓度变化 表示的平均反应速率为v(Z)= ;
(3)2min反应达平衡容器内混合气体的平均相对分子质量比起始时 (填增大、减小或不变);混合气体密度比起始时 (填增大、减小或不变)。
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X) =" n" (Y) =" n" (Z),则原混合气体中a : b = 。
(5)下列措施能加快反应速率的是 。
A.恒压时充入He
B.恒容时充入He
C.恒容时充入X
D.及时分离出Z
E.升高温度
F.选择高效的催化剂
(6)下列说法正确的是 。
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关 D.化学反应的限度是不可能改变的
E. 增大Y的浓度,正反应速率加快,逆反应速率减慢
【答案】(1)3X+Y![]() 2Z (2)0.05mol·L-1·min-1 (3)增大 不变
2Z (2)0.05mol·L-1·min-1 (3)增大 不变
(4)5:3 (5)CEF (6)AC
【解析】试题分析:(1) 由图像可知,X、Y随着时间的推移物质的量不断减少,X、Y为反应物,Z随着时间的推移物质的量不断增加,Z为生成物。平衡时由各物质转化的物质的量:X为0.3 mol,Y为0.1mol,Z为0.2mol可知化学方程式中各物质的化学计量数之比为3∶1∶2,则化学方程式为3X+Y![]() 2Z。
2Z。
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为v(Z)=0.2mol÷(2min×2L)=0.05mol·L-1·min-1 。
(3)根据M=m÷n,在恒容、密闭容器中,混合气体的质量不变,随着反应的进行n值变小,则2min反应达平衡容器内混合气体的平均相对分子质量比起始时增大。由于反应前气体的质量和容器容积均不变,则混合气体密度不变。
(4)根据上述分析可知
3X+Y![]() 2Z
2Z
起始量(mol) a b 0
变化量(mol) 3n n 2n
平衡量(mol) a-3n b-n 2n
根据题意:b-n=2n,b=3n,a-3n=2n,a=5n,解得a:b=5:3。
(5)A.恒压时充入He,导致气体体积增大,各物质的浓度降低,化学反应速率减慢,B.恒容时充入He,各物质的浓度不变,化学反应速率不变,C.恒容时充入X,导致反应物浓度增大,化学反应速率加快,D.及时分离出Z,导致生成物浓度降低,化学反应速率减慢;E.升高温度能加快化学反应速率,F.选择高效的催化剂能加快化学反应速率,答案选CEF。
(6)A.任何化学反应都有热效应,升高温度,平衡发生移动,所以升温能改变化学反应限度,A正确;B.升高温度,能加快正逆反应速率,只是增加的幅度不同,B错误;C.化学反应的限度与时间长短无关,C正确;D.改变外界条件,例如升高温度,平衡发生移动,所以化学反应的限度是可以改变的,D错误;E.增大Y的浓度,正反应速率加快,逆反应速率也加快,E错误;答案选AC。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 用白醋除铁锈:Fe2O3·xH2O+6H+==(3+x)H2O+2Fe3+
B. 用惰性电极电解 MgCl2溶液:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C. 向NH4Al(SO4)2 溶液中加入过量的 NaOH溶液:Al3++4OH-==AlO2-+2H2O
D. 向含NH3的污水中加入NaClO将其转化为N2:3ClO-+2NH3==3Cl-+N2↑+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列既属于放热反应又属于氧化还原反应的是
A. 氧化钙与水反应B. 铁丝在氧气中燃烧
C. NaOH溶液与盐酸反应D. Ba(OH)2·8H2O晶体与NH4Cl晶体反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A分子式为C8H8O2分子中苯环(C6H5—)上只有一个取代基,其红外光谱与核磁共振氢谱如下图。关于A的下列说法中,正确的是( )

A. 核磁共振氢谱数据在推理A的结构式时用处不大 B. A的结构式可表示为C6H5-COOCH3
C. 符合题中A分子结构特征的有机物有2种 D. 碥定A的分子结构还需要实验数据
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述的一定是金属元素的是
A. 易失去电子的物质 B. 能与酸反应的物质
C. 原子最外电子层只有一个电子的元素 D. 原子核内有11个质子的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一些晶体中的某些结构,请回答下列问题:

(1)代表金刚石的是(填字母编号,下同)______,其中每个碳原子与_____个碳原子最近且距离相等.
(2)代表石墨的是_____,每个正六边形占有的碳原子数平均为_____个.
(3)代表NaCl的是____,每个Na+周围与它最近且距离相等的Na+有_____个.
(4)代表CsCl的是_____,每个Cs+与_____个Cl﹣紧邻.
(5)代表干冰的是_____,每个CO2分子与______个CO2分子紧邻.
(6)已知石墨中碳碳键的键长比金刚石中碳碳键的键长短,则上述五种物质熔点由高到低的排列顺序为______(用字母编号回答).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有 Al2(SO4)3 ,FeSO4,CuCl2, NaOH四种溶液,将其两两反应,若有一种溶液滴入另两种溶液中均产生了白色沉淀,继续滴加该溶液,原白色沉淀或消失或发生颜色变化,则可推断这一种溶液是 ( )
A.Al2(SO4)3 B.FeSO4 C.BaCl2 D.NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3物质结构与性质] T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
元素 | 相关信息 |
T | T元素可形成自然界硬度最大的单质 |
W | W与T同周期,核外有一个未成对电子 |
X | X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol |
Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
Z | Z的一种同位素的质量数为63,中子数为34 |
(1)TY2是一种常用的溶剂,是 (填极性分子或非极性分子),分子中存在 个σ 键。W的最简单氢化物容易液化,理由是 。
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 。
(3)基态Y原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。Y、氧、W元素的第一电离能由大到小顺序为 (用元素符号作答)。
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00 g/cm3,则晶胞边长为 ;ZYO4常作电镀液,其中YO42-的空间构型是 ,其中Y原子的杂化轨道类型是 。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是

A.O2是 氧化剂
B.HO2 是氧化产物
C. HO2在碱中能稳定存在
D.1 mol Z参加反应有1 mol电子发生转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质与NaOH醇溶液共热可制得烯烃的是( )
A. C6H5CH2ClB. (CH3)3CCH2Br
C. CH3CHBrCH3D. CH3Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com